422 analisis de un diagrama de fases
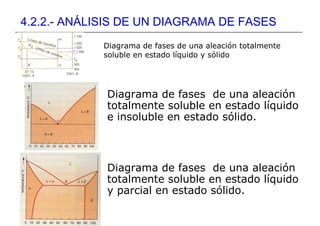
- 1. 4.2.2.- ANÁLISIS DE UN DIAGRAMA DE FASES Diagrama de fases de una aleación totalmente soluble en estado líquido y sólido Diagrama de fases de una aleación totalmente soluble en estado líquido e insoluble en estado sólido. Diagrama de fases de una aleación totalmente soluble en estado líquido y parcial en estado sólido.
- 2. 4.3.- DIAGRAMA Fe-C http://www2.ing.puc.cl/icmcursos/metalurgia/apuntes/cap1/18/ La distribución del diagrama es la siguiente: Hierro puro De 0% C a 0,008% C Aceros Desde 0,008 %C hasta 1,76 % C C < 0,89 %: acero hipoeutectoide. C > 0,89 %: acero hipereutectoide Fundiciones De 1,76% C a 6,67 % C En el diagrama Fe-C, sólo se llega al 6,67 % de C. Con este porcentaje se forma cementita (Fe3C, carburo de hierro) que es un material duro y frágil. Por encima de este porcentaje, el carbono precipita como grafito y no se usa industrialmente.
- 4. • A, B, C y D línea de liquidus • A, H, J, E, F y D línea de solidus. 1499 punto peritéctico (J) 1.499°C se forma la austenita contenido de C entre 0,1% y 0,5%. Punto eutéctico (C) 1.147°C se forma ledeburita (austenita +cementita) contenido de C superior al 2,14%. 1147 punto eutectoide (O) 720°C se forma perlita (ferrita +cementita) contenido de C superior al 0,2%. 720 0,8 2,14 4,3 6,67
- 5. 1499 Punto eutéctico (C) 1.147°C se forma ledeburita (austenita +cementita) contenido de C superior al 2,14%. 1147 punto eutectoide (O) 720°C se forma perlita (ferrita +cementita) contenido de C superior al 0,2%. 720 0,8 2,14 4,3 6,67
- 6. 4.3.1.- METALES FERROSOS Son aquellos que, como principal elemento, contienen hierro. (en latín ferrum: hierro) El hierro es el metal mas importante del sistema productivo y el segundo en abundancia (1º aluminio) (edificios, transportes, máquinas, ...) Características del hierro: Símbolo: Fe Punto de fusión: 1538ºC (antes de esta temperatura se vuelve pastoso y fácilmente se puede cambiar la forma mediante golpes) Resistencia a la tracción: 12kg/mm2 Densidad: 7,8kg/dm3 Se magnetiza fácilmente Dúctil y maleable Como las propiedades del hierro puro no son buenas, se mezcla con otros elementos.
- 7. 4.3.1.1- TIPOS DE METALES FERROSOS El hierro sólo se usa para fabricar objetos de forja y núcleos de electroimanes. Generalmente se combina con carbono para mejorar sus aplicaciones. Material Composición Características Más duro que hierro Acero hierro+carbono (C<2%) Fácil de soldar Acero hierro+carbono+cromo Resistente a la corrosión inoxidable Hierro colado hierro+mucho carbono Hacer piezas por moldeo o Fundición (C>2%)
- 8. 4.3.1.2- TIPOS DE ACEROS aceros no aleados Contienen otros metales en proporción inferior al 1%. Son duros, tenaces, dúctiles y maleables. Se emplean para fabricar tornillos, bisagras y planchas de carrocería. aceros de baja aleación Contienen otros metales en proporción comprendida entre el 1 % y el 5 %. Son muy duros y tenaces pero menos dúctiles que los no aleados. Se emplean para fabricar herramientas y rodamientos. aceros de alta aleación Contienen otros metales cuya proporción supera el 5%. Son medianamente duros y muy resistentes a la oxidación. El más conocido es el acero inoxidable, que tiene muchas aplicaciones: depósitos, cubiertos, etc.
- 9. 4.3.2.- REPRESENTACIÓN DIAGRAMA Fe-C
- 10. En la solidificación aparece una solución sólida llamada austenita para proporciones inferiores al 1,76% de carbono, y con un 4,30% se crea un eutéctico llamado ledeburita. Esto provoca la primera clasificación del sistema hierro-carbono: se habla de aceros si la proporción de carbono es inferior a 1,76%, y de fundiciones para proporciones entre 1,76 y 6,67%. La austenita también se llama hierro-γ, y tiene una red cúbica centrada en las caras (FCC) que en su interior admite átomos de carbono. Pero cuando se contrae la red al disminuir la temperatura, disminuye la solubilidad como ya sabemos, y se expulsa el carbono sobrante en forma de cementita. Cuando la temperatura baja hasta 723° C el hierro sufre un cambio alotrópico y su red se transforma en cúbica centrada en el cuerpo (BCC), que no acepta apenas átomos de carbono en su seno; entonces el hierro se denomina ferrita o hierro-α. Este cambio de solubilidad en estado sólido conlleva la formación de un eutectoide llamado perlita con una concentración de 0,89% de carbono que está formado por láminas de ferrita y de cementita. A los aceros que tienen una proporción menor que 0,89% de carbono se les denomina hipoeutectoides, y si tienen entre 0,89 y 1,76% de carbono, hipereutectoides.
- 11. 4.3.3.- COMPOSICIÓN DE LAS ALEACIONES Fe-C a) Ferrita: Solución sólida de carbono en hierro α. Solubilidad pequeña a temperatura ambiente, (disuelve como máximo el 0,008% de carbono). Por esta razón, se considera a la ferrita como hierro α puro. Es el más blando y dúctil constituyente de los aceros. Tiene una dureza de 90 HB y una resistencia a la rotura de 28 kg/mm2, puede sufrir alargamientos del 30 al 40%, y posee propiedades magnéticas. b) Cementita o carburo de hierro (Fe3C) Es el constituyente más duro y frágil de los aceros, puede alcanzar una dureza de 800 HB, tiene propiedades magnéticas hasta los 210°C, y a partir de esta, temperatura pierde las propiedades magnéticas. c) Perlita Está formada por 86,5% de ferrita y 13,5% de cementita. Tiene una dureza de 200 HB, una resistencia a la rotura de 80 kg/mm2, y un alargamiento del 15%. d) Austenita Está formada por una solución sólida por inserción de carbono en hierro γ. La proporción de carbono disuelto varía desde el 0 al 1,76%. Es el constituyente más denso de los aceros. Su dureza puede alcanzar los 300 HB, una resistencia de 100 kp/mm2, y un alargamiento de un 30%. No es magnética.