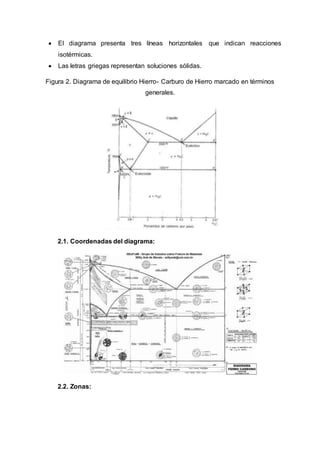
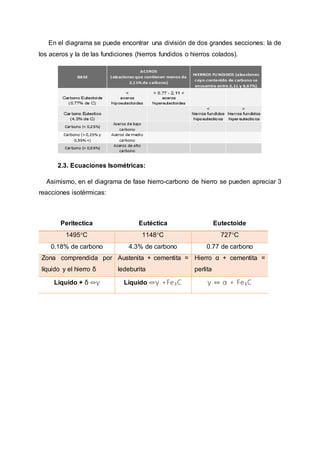
Este documento presenta información sobre el hierro y el diagrama de equilibrio hierro-carburo de hierro. Explica las propiedades del hierro, sus tipos de aleaciones como aceros y fundiciones, y las diferentes zonas del diagrama como la región delta y austenita. También describe las líneas y puntos clave del diagrama, como la línea peritectica y la solubilidad máxima de hierro delta.

![1. El Hierro:
1.1. Definición:
El Hierro es un metal que puede presentarse en diversas variedades de estructuras
cristalinas, es un elemento químico de aspecto metálico brillante con un tono grisáceo
con número atómico 26. Su símbolo es Fe y pertenece al grupo de los metales de
transición y su estado habitual en la naturaleza es sólido.
1.2. Constitución:
La masa atómica de un elemento está determinada por la masa total de neutrones
y protones que se puede encontrar en un solo átomo perteneciente a este elemento.
En cuanto a la posición donde encontrar el hierro dentro de la tabla periódica de los
elementos, el hierro se encuentra en el grupo 8 y periodo 4. El hierro tiene una masa
atómica de 55,845 u.
La configuración electrónica del hierro es [Ar]3d64s2. La configuración electrónica
de los elementos, determina la forma en la cual los electrones están estructurados en
los átomos de un elemento. El radio medio del hierro es de 140 pm, su radio atómico
o radio de Bohr es de 156 pm y su radio covalente es de 126 pm. El hierro tiene un
total de 26 electrones cuya distribución es la siguiente: En la primera capa tiene 2
electrones, en la segunda tiene 8 electrones, en su tercera capa tiene 14 electrones
y en la cuarta, 2 electrones.
1.3. Características:
A continuación, puedes ver una tabla donde se muestra las principales
características que tiene el hierro.
Hierro
Símbolo químico Fe
Número atómico 26
Grupo 8
Periodo 4
Aspecto metálico brillante con un tono grisáceo
Bloque d
Densidad 7874 kg/m3](https://image.slidesharecdn.com/diagramahierrocarbono-210718035054/85/Diagrama-Hierro-Carbono-2-320.jpg)
![Masa atómica 55.845 u
Radio medio 140 pm
Radio atómico 156
Radio covalente 126 pm
Configuración electrónica [Ar]3d64s2
Electrones por capa 2, 8, 14, 2
Estados de oxidación 2, 3
Óxido anfótero
Estructura cristalina cúbica centrada en el cuerpo
Estado sólido
Punto de fusión 1808 K
Punto de ebullición 3023 K
Calor de fusión 13.8 kJ/mol
Presión de vapor 7,05 Pa a 1808 K
Electronegatividad 1,83
Calor específico 440 J/(K·kg)
Conductividad eléctrica 9,93·106S/m
Conductividad térmica 80,2 W/(K·m)
1.4. Tipos de aleaciones del hierro:
Aceros:
Los aceros son una aleación del hierro, es decir, una combinación entre hierro y
carbono. El máximo contenido de carbono que puede tener el acero es del 2%. Se
clasifican según su contenido de carbono:
Acero bajo en carbono. Contiene menos del 0,25%. Es dúctil y ofrece alta
resistencia mecánica.
Acero medio carbono. Contiene entre 0,25% y 0,6 %. Es menos dúctil pero
más resistente, por lo que se utiliza en piezas mecánicas que deben resistir el
desgaste.
Acero alto carbono. Contiene entre 0,6% y 1,4%. Es un material muy duro
que se utiliza en herramientas.](https://image.slidesharecdn.com/diagramahierrocarbono-210718035054/85/Diagrama-Hierro-Carbono-3-320.jpg)