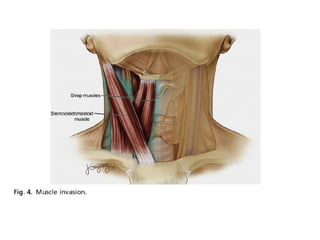
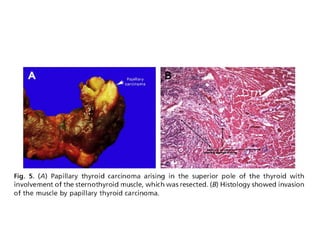
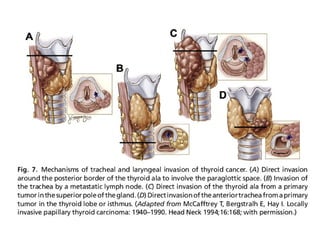
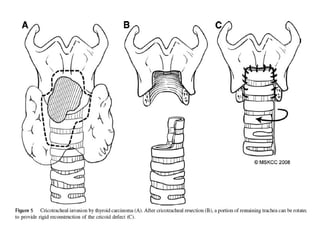
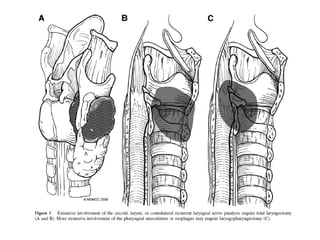
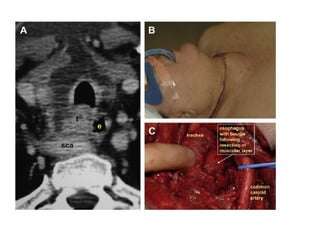
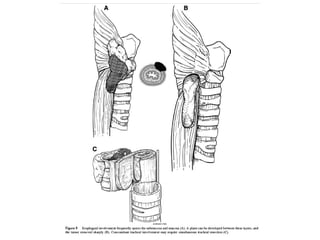
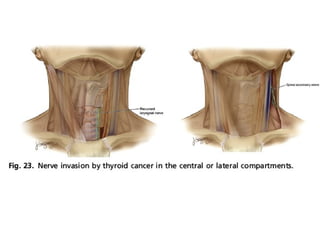
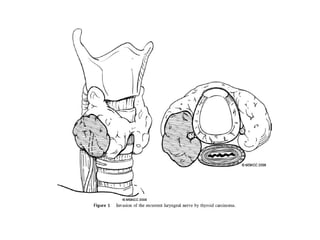
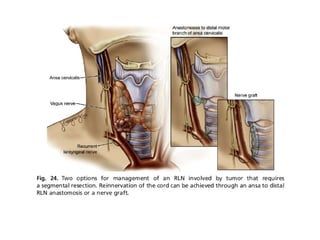
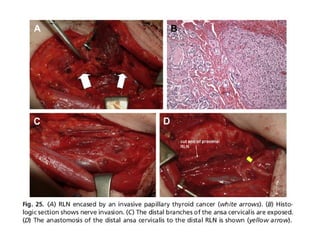
Este documento resume la información sobre el cáncer de tiroides avanzado. Describe las estructuras que pueden verse afectadas por la extensión local del tumor, como los músculos pre-tiroideos, el complejo laringotraqueal, el esófago y los nervios recurrentes laríngeos. También discute los diferentes enfoques quirúrgicos para resecar el tumor y preservar la función de acuerdo con la extensión de la enfermedad.








































![ Soo-Youn An, K. H. (2010). Surgical management of locally
advanced thyroid cancer. Current Opinion in Otolaryngology
and Head and Neck Surgery , 119-123.
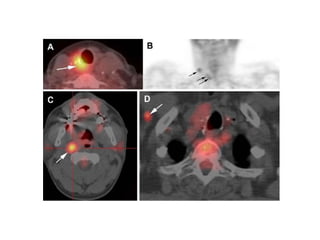
Taieb, D. (2011). [18F] Fluorodeoxyglucose positron emission
tomography in advanced thyroid cancer. Medicine Nucleaire ,
329-331.
Urken, M. L. (2010). Prognosis and Management of Invasive
Well-differentiated Thyroid Cancer. Otolaryngol Clin N Am ,
301-328.
Yassine Lalami, A. A. (2011). Recurrent thyroid cancer: a
molecular-based therapeutic breakthrough. Current Opinion in
Oncology , 235-240.](https://image.slidesharecdn.com/caavanzadodetiroides-130115231231-phpapp01/85/Ca-avanzado-de-tiroides-76-320.jpg)
