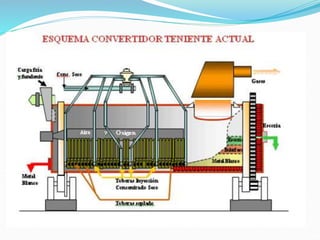
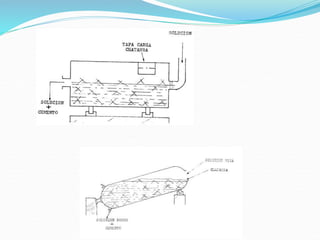
El documento proporciona información sobre las propiedades, usos, minerales, procesos de extracción y refinación del cobre. Describe los principales métodos para procesar minerales de cobre, incluyendo flotación, tostación, fusión, conversión y lixiviación, así como técnicas de purificación como la extracción con disolventes, cementación y electrorefinación.