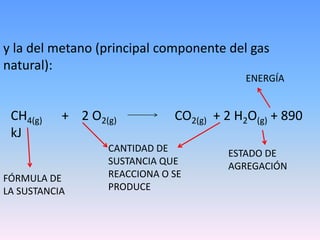
La combustión es un fenómeno químico en el que se desprende energía en forma de luz y calor. Para que ocurra la combustión se necesita un combustible, un comburente como el oxígeno, y alcanzar la temperatura de inflamación. La combustión puede ser completa, produciendo dióxido de carbono y agua, o incompleta, generando también monóxido de carbono y hollín.