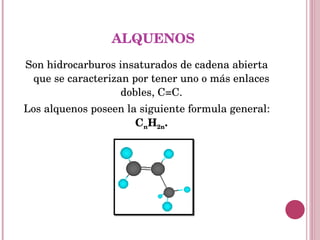
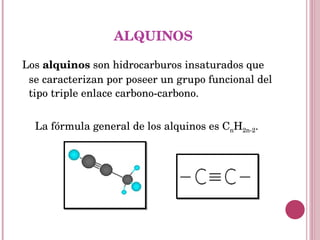
Los alcanos son hidrocarburos saturados formados por enlaces simples entre átomos de carbono e hidrógeno. Los alquenos contienen enlaces dobles carbono-carbono y los alquinos enlaces triples. Los alcanos son generalmente no reactivos mientras que los alquenos y alquinos son más reactivos. Todos ellos tienen usos importantes como combustibles, plásticos, disolventes y en la industria química.