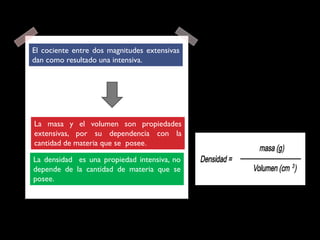
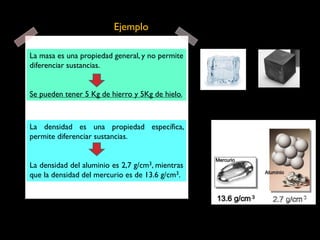
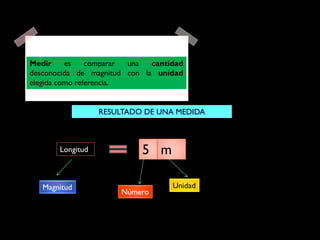
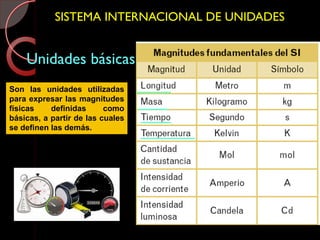
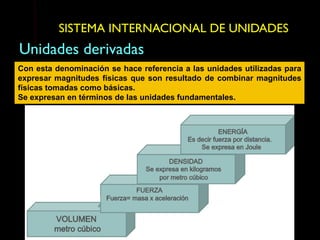
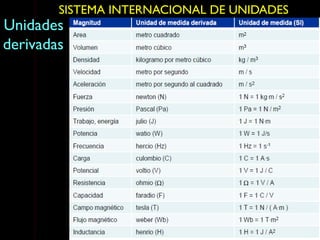
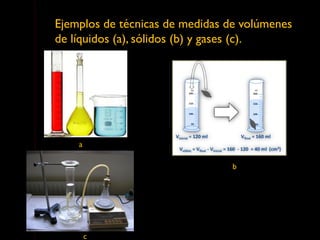
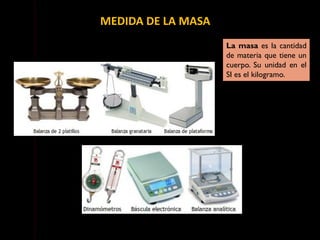
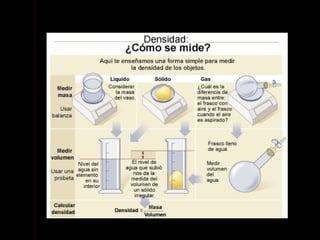
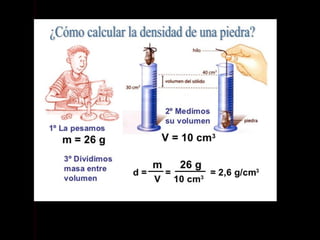
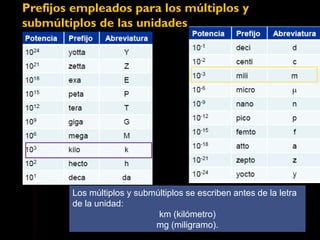
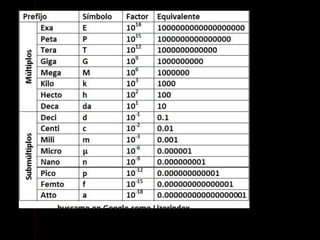
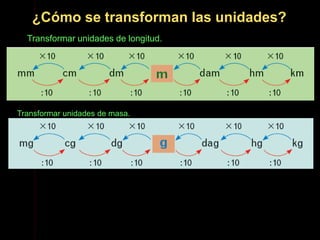
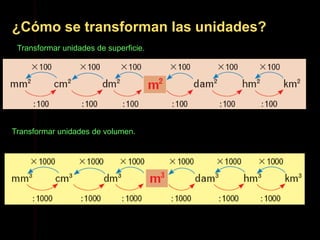
Este documento describe las propiedades de la materia, incluyendo su definición, propiedades y cómo se puede medir. Explica que la materia tiene masa y volumen y que se puede medir utilizando el Sistema Internacional de Unidades, con unidades como el kilogramo y el metro cúbico. También cubre conceptos como densidad, volumen, masa y cómo transformar entre diferentes unidades de medida.