1) El documento describe varios tipos de meteorización que afectan a las rocas, incluyendo la meteorización física, química y biológica.
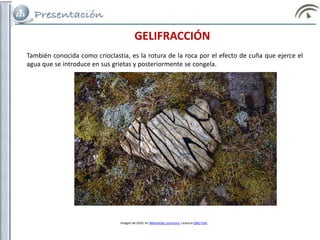
2) Dentro de la meteorización física se encuentran procesos como la descompresión, termoclastia, gelifracción y haloclastia.
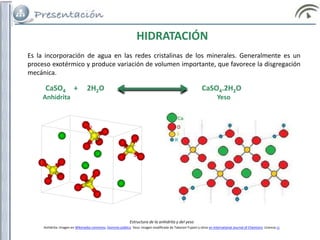
3) La meteorización química incluye procesos como la hidratación, oxidación-reducción, hidrólisis, disolución, carbonatación y biológica.