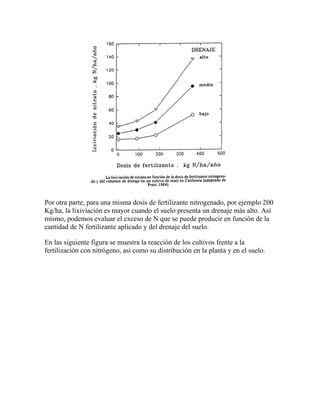
El documento habla sobre la contaminación por fertilizantes de nitrógeno. Explica que el nitrógeno es un nutriente esencial para las plantas y que se encuentra en el suelo en formas orgánicas e inorgánicas. También describe el ciclo del nitrógeno en el suelo, incluyendo la fijación, nitrificación, reducción y desnitrificación. Finalmente, discute los impactos ambientales del exceso de fertilizantes de nitrógeno, como la lixiviación de nitratos que puede contaminar aguas sub