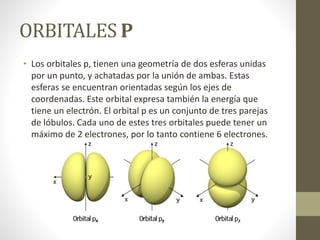
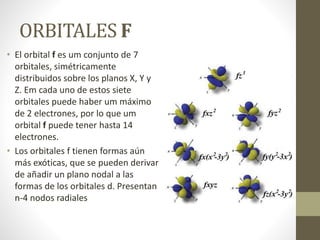
Este documento describe los orbitales atómicos y los electrones. Explica que los electrones orbitan alrededor del núcleo en espacios llamados orbitales agrupados en niveles de energía. Describe los cuatro tipos básicos de orbitales (s, p, d, f) y proporciona ejemplos de sus formas. También explica la configuración electrónica del átomo de neón como ejemplo.