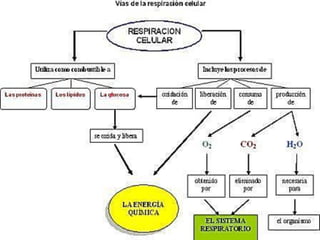
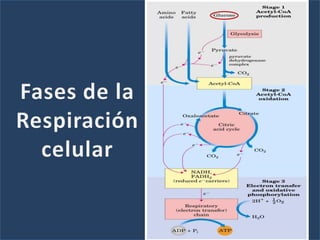
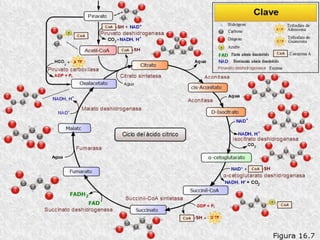
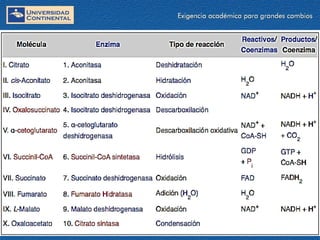
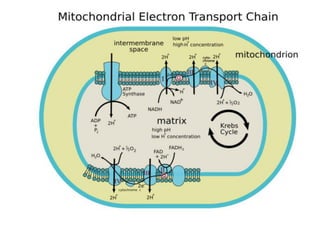
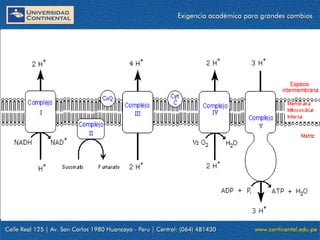
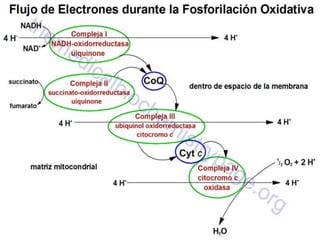
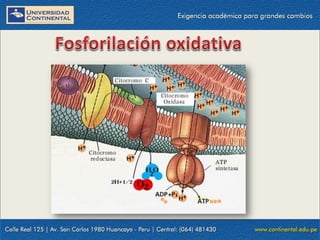
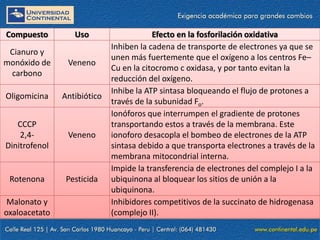
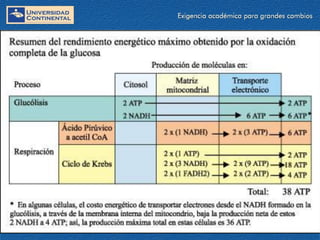
El documento describe los procesos de la respiración celular y el ciclo de Krebs. El ciclo de Krebs produce acetil-CoA y dos moléculas de CO2 a través de una serie de reacciones. Cada molécula de glucosa que ingresa al ciclo de Krebs produce 32 moléculas de ATP a través de la fosforilación oxidativa. El ciclo está sujeto a retroalimentación negativa por la unión de ATP y NADH.