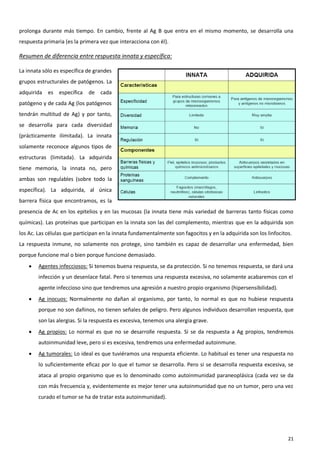
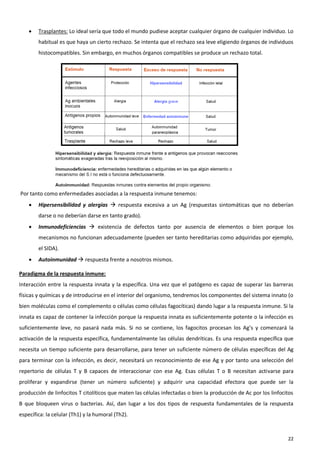
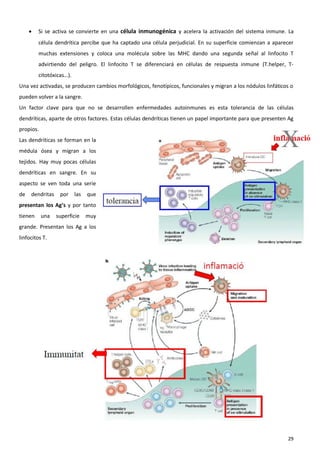
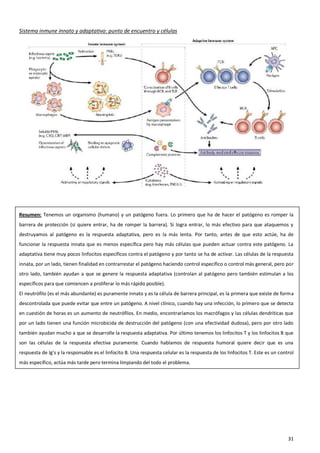
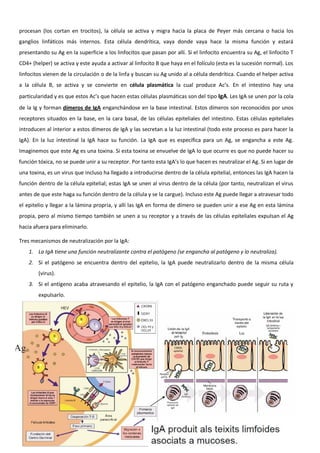
El sistema inmune es una respuesta coordinada que involucra múltiples células y moléculas para defender al organismo de agentes extraños como bacterias y virus. Cuando se presenta un antígeno, el sistema inmune lo reconoce y desarrolla una respuesta específica para combatir el patógeno, involucrando órganos linfoides donde se generan las células inmunes, así como linfocitos, células fagocíticas y otros componentes celulares que trabajan de forma conjunta.