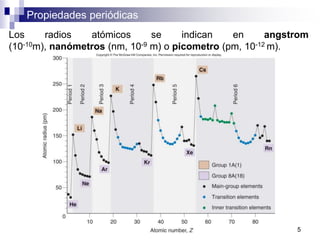
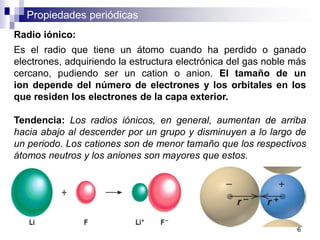
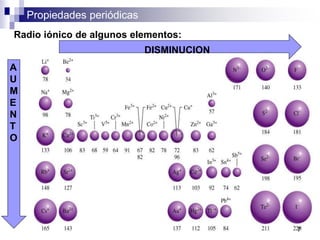
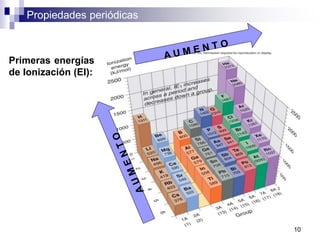
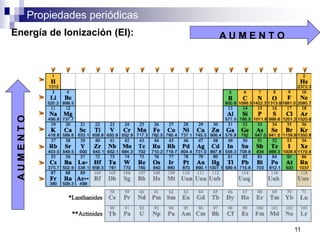
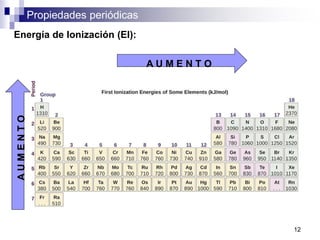
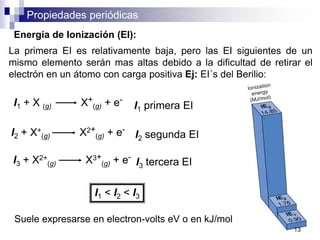
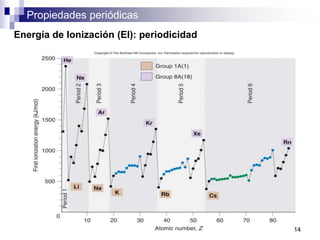
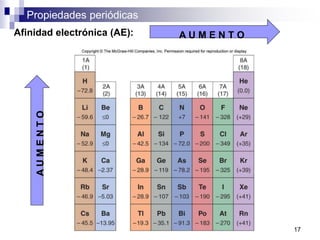
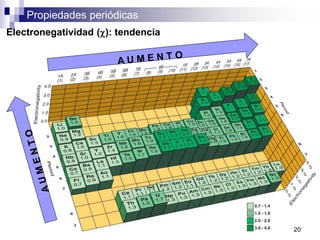
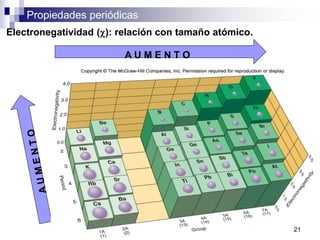
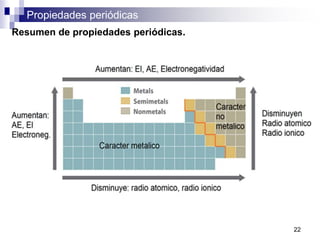
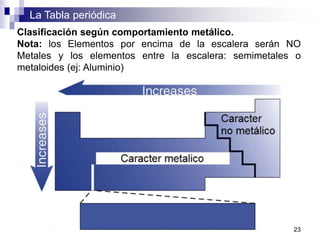
Este documento presenta las principales propiedades periódicas como el radio atómico, radio iónico, energía de ionización, afinidad electrónica y electronegatividad. Explica que estas propiedades varían de forma gradual a lo largo de los períodos y grupos de la tabla periódica. También describe las tendencias en el cambio de estas propiedades y cómo se relacionan entre sí para determinar el tipo de enlace entre los elementos.