Teoría sobre la replicación genéticaaaaa
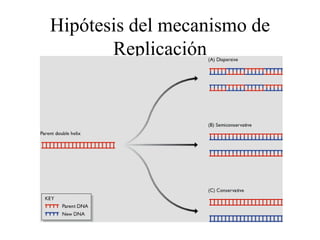
- 1. Hipótesis del mecanismo de Replicación
- 2. DNA marcado con 15N y 14N separado por un gradiente de densidad (a) (b)
- 3. Experimento de Hersey y Chase
- 5. Replicación de un cromosoma circular tomando la forma de (a) (b)
- 6. Modelos de replicación en DNA circular
- 7. El proceso de la replicación • Iniciación. Involucra el reconocimiento de la posición en dónde empieza la replicación de una molécula de DNA. • Elongación. Eventos de la horquilla de replicación en dónde es sintetizada una hebra complementaria. • Terminación. Poco entendia
- 8. Iniciación • No es un proceso al azar. • Empieza en una secuencia conocida como origen de replicación • Generalmente se inician dos horquillas de replicación de cada origen (bidireccional). • Un genoma circular bacteriano presenta un solo origen de replicación. • En eucariontes hay multiples orígenes para cada cromosoma. (levadura ~300).
- 10. Esquema de la autoradiografía de una horquilla de replicación
- 11. Inicio de la replicación en E. coli • El origen de replicación de E.coli se conoce como oriC. • Presenta 245 pb de DNA. • Contiene dos motivos cortos repetidos, uno de nueve nucleótidos (nonámero), cinco copias y otro de 13 nucleótidos (tridecámero) 3 copias.
- 13. Inic de replicación en E. coli
- 15. • La proteína DnaA se une cerca de las regiones ricas en AT en una región de reconocimiento. • DnaA debe estar acoplada a ATP. • 30 moléculas de DnaA se unen a oriC • La unión ocurre cuando el DNA esta superenrollado negativamente, situación normal en E. coli.
- 16. • El resultado de la unión de DnaA a la doble hélice es que ésta se funde. • El mecanismo exacto no se conoce pero parece ser el estrés de torción inducido por DnaA. • La fusión de la hélice es promovida por HU, la proteína más abundante que ayuda a empacar al DNA de E. coli.
- 17. • Después de la fusión son reclutadas las proteínas DnaBC, formando el complejo pre-priming. • DnaC tiene un papel transitorio y puede ser que ayude a DnaB a unirse. • DnaB es una helicasa, que puede romper pares de bases. • Incrementa la región de hebra sencilla en el origen.
- 18. Orígenes de replicación el levadura • Se les llama ARSs (autonomously replicating sequences) • 200 pb • Presenta regiones discretas o subdominios • ORS (secuencia de reconocimiento del origen), 40 pb que es reconocida por un grupo de 6 proteínas, el ORC (complejo de reconocimiento del origen). • No es precisamente un complejo de iniciación pues sigue unido después de iniciada la replicación.
- 19. Estructura del origen de replicación de levadura
- 20. Origen de replicación en eucariontes superiores • No se ha podido encontrar secuencias ni homólogas ni análogas a orígenes de replicación en eucariontes superiores. • Podría ser que la replicación se iniciara en estructuras proteínicas que tienen posiciones específicas en el núcleo.
- 21. • Se describió por Aladjem et al., (1998) una región de 8 kb que conservó su potencialidad de iniciar la replicación a alta frecuencia al clonarla en genoma de chimpancés. • Proteínas con secuencias homólogas a ARSs se han encontrado también.
- 22. Elongación o alargamiento • Dificultades – Las dos hebras tienen que ser copiadas al mismo tiempo y la polimerasa solo copia de 5’--> 3’ – La hebra retardada debe copiarse de manera discontinua produciendo fragmentos cortos. – La DNA polimerasa necesita cebadores que proporcionen extremos 3’
- 23. DNA pol en eucariontes y procariontes • Sintetizan polinucleótidos en sentido 5’-->3’ • Tienen actividad de exonucleasa 3’-- >5’ (no todas)
- 24. Sintesis de DNA dependiente de un molde
- 25. DNA polymerases involved in replication of bacterial and eukaryotic genomes Exonuclease activities Enzyme Subunits 3’-->5’ 5’-->3’ Function Bacterial DNA polymerase DNA polymerase I 1 Yes Yes DNA repair, replication DNA polymerase III At least 10 Yes No Main replicating enzyme Eukaryotic DNA polymerases DNA polymerase a 4 No No Priming during replication DNA polymerase g 2 Yes No Mitochondrial DNA replication DNA polymerase d 2 or 3 Yes No Main replicative enzyme DNA polymerase e At least 1 Yes No Required for detection of DNA damage during genome replication DNA polymerase k 1 or 2? ? ? Required for attachment of cohesin proteins which hold sister chromatids together until the anaphase stage of nuclear division Bacteria and eukaryotes possess other DNA polymerases involved primarily in repair of damaged DNA. These enzymes include DNA polymerases II, IV and V of Escherichia coli and the eukaryotic DNA polymerases b, ζ, η , q and ι. Repair processes are described in Section 14.2.
- 26. Gen estructural* Subunidades Mr Exonucleasa 3'-->5' (corrección de errores) Exonucleasa 5'-->3' Velocidad de polimerización (nucleótidos/s) Procesividad (nucleótidos añadidos antes de disociarse DNA polimerasas I pol A 1 103,000 Si aaaaa Si 16-20 aaa 3-200 II pol B ≥ 4 88,000 Sí aaaaa No ~7 a ≥10,000 III pol C ≥ 10 ~900,000 Síaa aaaaa No 250- 1000aaa ≥500,000 Comparación de las DNA pol de E. coli
- 27. Aislamiento de diferentes formas de actividad Pol III
- 28. Estructura de subunidad tau
- 29. DNA pol de eucariontes • Son al menos 9 polimerasas • Se nombran con letras griegas (igual que las subunidades de la pol III). • La replicasa es la d • Trabaja en conjunto con el antígeno nuclear de proliferación (PCNA) • PCNA equivale a la subunidad b de la DNA pol de E. coli.
- 30. Síntesis discontinua del DNA
- 31. Cebando la síntesis del DNA
- 32. Helicasa
- 33. Estructura de la helicasa
- 34. SSB
- 36. Síntesis en paralelo de la hebra líder y rezagada
- 37. Unión de los fragmentos de Okazaki
- 39. Dos modelos de acompletar la replicación resagada
- 41. Topología de la terminación en cromosomas circulares.
- 42. Secuencias de termino en e coli
- 43. Actividad de topoisomerasas • Las DNA topoisomerasas no desenrollan la doble hélice. • Lo que hacen es resolver el problema topológico contratacando el sobre-enrollamiento que de otra manera tendría la molécula por la progresión de la horquilla de replicación. • El resultado es que la hélice puede ser “unzipped” poniendo las dos hebras aparte sin que la molécula tenga que rotar.
- 44. Tipos de DNA topoisomerasas Type Substrate Examples Type IA Single-stranded DNA Escherichia coli topoisomerases I and III; yeast and human topoisomerase III; archaeal reverse gyrase Type IB Single-stranded DNA Eukaryotic topoisomerase I Type II Double-stranded DNA E. coli topoisomerases II (DNA gyrase) and IV; eukaryotic topoisomerases II and IV
- 45. Desenrollamiento de la cadena mediante topoisomerasas
- 46. Topoisomerasas tipo I y II
- 47. Coesinas
- 48. Problema del primer cebador
- 49. Extensión del cromosoma por la terlomerasa
- 50. Terminación de la expresnión
- 52. Sequences of telomere repeats and telomerase RNAs in various organisms Species Telomere repeat sequence Telomerase RNA template sequence Human 5’-TTAGGG-3’ 5’-CUAACCCUAAC-3’ Oxytricha 5’-TTTTGGGG-3’ 5’-CAAAACCCCAAAACC-3’ Tetrahymena 5’-TTGGGG-3’ 5’-CAACCCCAA-3’ Oxytricha and Tetrahymena are protozoans which are particularly useful for telomere studies because at certain developmental stages their chromosomes break into small fragments, all of which have telomeres: they therefore have many telomeres per cell (Greider, 1996).
- 53. Fases del ciclo celular
- 54. Cdc6 p