Óxidos.pdf
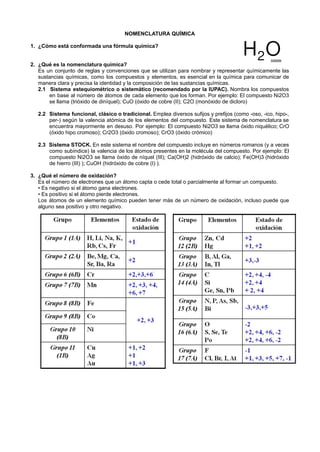
- 1. NOMENCLATURA QUÍMICA 1. ¿Cómo está conformada una fórmula química? 2. ¿Qué es la nomenclatura química? Es un conjunto de reglas y convenciones que se utilizan para nombrar y representar químicamente las sustancias químicas, como los compuestos y elementos, es esencial en la química para comunicar de manera clara y precisa la identidad y la composición de las sustancias químicas. 2.1 Sistema estequiométrico o sistemático (recomendado por la IUPAC). Nombra los compuestos en base al número de átomos de cada elemento que los forman. Por ejemplo: El compuesto Ni2O3 se llama (trióxido de diníquel); CuO (óxido de cobre (II); C2O (monóxido de dicloro) 2.2 Sistema funcional, clásico o tradicional. Emplea diversos sufijos y prefijos (como -oso, -ico, hipo-, per-) según la valencia atómica de los elementos del compuesto. Este sistema de nomenclatura se encuentra mayormente en desuso. Por ejemplo: El compuesto Ni2O3 se llama óxido niquélico; CrO (óxido hipo cromoso); Cr2O3 (óxido cromoso); CrO3 (óxido crómico) 2.3 Sistema STOCK. En este sistema el nombre del compuesto incluye en números romanos (y a veces como subíndice) la valencia de los átomos presentes en la molécula del compuesto. Por ejemplo: El compuesto Ni2O3 se llama óxido de níquel (III); Ca(OH)2 (hidróxido de calcio); Fe(OH)3 (hidróxido de hierro (III) ); CuOH (hidróxido de cobre (I) ). 3. ¿Qué el número de oxidación? Es el número de electrones que un átomo capta o cede total o parcialmente al formar un compuesto. • Es negativo si el átomo gana electrones. • Es positivo si el átomo pierde electrones. Los átomos de un elemento químico pueden tener más de un número de oxidación, incluso puede que alguno sea positivo y otro negativo.
- 2. LOS ÓXIDOS Los óxidos son compuestos binarios, es decir que sólo tienen dos elementos, de los cuales uno es el oxígeno actuando con estado de oxidación -2. El otro elemento, metal o no metal, actúa con estado de oxidación positivo. Cuando se trata de un metal, el óxido formado se conoce como óxido básico; cuando es un no metal, óxido ácido. Clasificación de los óxidos básicos 1. Óxidos básicos Son óxidos de metales - La unión entre el oxígeno y el metal se produce a través de una unión iónica - Existen como redes cristalinas. Cuando se escribe la fórmula química de un óxido básico, el metal debe colocarse delante del oxígeno. Seguidamente, se colocan los subíndices que corresponden a los números de oxidación de cada elemento, pero intercambiados y, por último, si son múltiplos, se simplifican. Ejemplo1 : Óxido de potasio K (+1) O ( -2) Ejemplo1 : Óxido de hierro Fe (+2) O ( -2) Ejercicios 1. Realizar ejercicios con elementos del grupo 1 y grupo 2. 2. Con manganeso.