Experimentos con co2 solido para secundaria
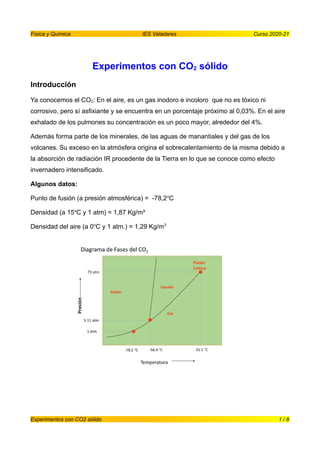
- 1. Física y Química IES Valadares Curso 2020-21 Experimentos con CO2 sólido Introducción Ya conocemos el CO2: En el aire, es un gas inodoro e incoloro que no es tóxico ni corrosivo, pero sí asfixiante y se encuentra en un porcentaje próximo al 0,03%. En el aire exhalado de los pulmones su concentración es un poco mayor, alrededor del 4%. Además forma parte de los minerales, de las aguas de manantiales y del gas de los volcanes. Su exceso en la atmósfera origina el sobrecalentamiento de la misma debido a la absorción de radiación IR procedente de la Tierra en lo que se conoce como efecto invernadero intensificado. Algunos datos: Punto de fusión (a presión atmosférica) = -78,2o C Densidad (a 15o C y 1 atm) = 1,87 Kg/m³ Densidad del aire (a 0o C y 1 atm.) = 1,29 Kg/m3 Experimentos con CO2 sólido 1 / 8
- 2. Física y Química IES Valadares Curso 2020-21 La nieve carbónica también llamado hielo seco es dióxido de carbono CO2 en estado sólido. El nombre de hielo seco es debido a que al calentarse no pasa por el estado líquido, si no que directamente se produce el cambio de estado de sólido a gas. A este proceso de cambio de estado de sólido a gas, se conoce como sublimación. Para la producción de nieve carbónica, primero se licua el gas sometiéndolo a una presión muy elevada y a continuación, se deja que el líquido se expansione a presión atmosférica, con lo que su temperatura desciende y el resultado es la formación de la nieve carbónica, que una vez extraída de la cámara de expansión se comprime mecánicamente para formar bloques de forma cilíndrica. El producto así obtenido se aplica en múltiples procesos, por ejemplo: • Refrigeración: Tiene por objeto enfriar alimentos, conservar determinadas sustancias perecederas, pieles, productos farmacéuticos, etc. En reacciones químicas en laboratorios para evitar reacciones exotérmicas se emplea hielo seco como refrigerante. • Extintores de incendios: En estos aparatos se almacena el gas en forma líquida a presión elevada. Al descargarse se solidifica parcialmente formando copos blancos, por lo que estos extintores se llaman de nieve carbónica. Apaga principalmente por sofocación, desplazando el oxígeno del aire y produciendo a la vez un enfriamiento. Experimentos con CO2 sólido 2 / 8
- 3. Física y Química IES Valadares Curso 2020-21 • Criocirugía: La nieve carbónica puede producir temperaturas adecuadas para el tratamiento de lesiones cutáneas benignas y superficiales (para las que se requieren temperaturas de –20 ºC), tales como las verrugas o la queratosis solar, aunque no son tan eficaces como el nitrógeno líquido para destruir los cánceres cutáneos. • Abono carbónico: El aumento del contenido de CO2 en el aire de los invernaderos conduce a la estimulación del crecimiento de las plantas; esto se puede conseguir colocando pedazos de hielo seco. Para la mayoría de hortalizas el contenido más favorable resulta de 0,2 a 0,3% en volumen, en contraste con el contenido “natural” 0,03% en volumen. • Investigación médica y científica: Para conservar órganos para trasplantes o estudios es muy recomendable utilizar el hielo seco, puesto que su gran capacidad de refrigeración hace que se conserve en buen estado. • En restauración: En la alta cocina se emplea el hielo seco para e crear platos totalmente exóticos y de una alta calidad y precio. • Industria: En la industria se utiliza este elemento para facilitar el ensamblaje y ajuste de piezas por contracción por frío. • Como conservante: Cuando se produce su sublimación se genera una atmósfera cuya concentración de CO2 es tan alta, que se ejerce una acción antimicrobiana. Por ello, es un excelente gas para ralentizar el desarrollo de las bacterias, mohos y levaduras y crean un ambiente totalmente desinfectado. Este gas es capaz de desplazar el oxígeno presente en la atmósfera, en interior de envases y en contenedores, lo que contribuye a mejorar la calidad biológica de los lugares donde se necesita guardar y preservar determinados productos. Experimentos con CO2 sólido 3 / 8
- 4. Física y Química IES Valadares Curso 2020-21 Medidas de seguridad Tocar hielo seco con la piel sin proteger puede llevar a la congelación instantánea, y respirar demasiado su niebla de dióxido de carbono puede provocar asfixias. Por eso es muy importante manipularlo con pinzas y mantener el hielo seco en un lugar bien ventilado y siempre con supervisión de la profesora. Por supuesto no debe comerse, ni beber ninguna bebida enfriada con él, porque no está garantizada su higiene sanitaria (recordemos que proviene de un laboratorio de investigación de la Universidad de Vigo). Nunca se debe almacenar el hielo seco en recipientes herméticos. La temperatura cálida provoca la formación de grandes cantidades de gas. Esto puede conducir a la explosión del recipiente. Los contenedores de hielo seco deben tener válvula para respirar. Experimentos Experiencia 1: Deslizar un trozo de nieve carbónica sobre una superficie Material: nieve carbónica. Si se coloca un trozo sobre una superficie lisa y se le da un ligero impulso, el hielo seco se desliza casi sin rozamiento. Cuestión: ¿Porqué ocurre eso? Experiencia 2: Introducir un trozo de nieve carbónica en un vaso con agua Material: nieve carbónica, vaso de precipitado, agua. Al introducir un trozo de nieve carbónica en un vaso de agua (si está caliente el efecto se verá intensificado) se produce un intenso burbujeo y se forman "humos" blancos que se deslizan por el exterior del recipiente hacia abajo. Cuestiones: ¿Si el gas CO2 es incoloro, que es el humo blanco que se forma? ¿Qué cambios de estado están teniendo lugar? ¿Porqué se desliza hacia abajo? Experiencia 3: Apagando velas Material: nieve carbónica, vaso de precipitado con velas de distintos tamaños, cerillas. Al volcar suavemente el recipiente con nieve carbónica sobre las velas, estas se irán apagando. Cuestión: ¿Porqué ocurre esto? Experimentos con CO2 sólido 4 / 8
- 5. Física y Química IES Valadares Curso 2020-21 Experiencia 4: Jugando con globos Material: nieve carbónica, globos. Al introducir un trozo de nieve carbónica en un globo y cerrarlo posteriormente se aprecia cómo el globo se infla lentamente sin que en su interior aparezcan gotas de líquido, y además este globo así inflado no puede ascender espontáneamente. Cuestión: ¿Porqué este globo se hincha pero no asciende? ¿Porqué no hay gotas en el interior del globo? Experiencia 5: Pompas de jabón. Material: nieve carbónica, vaso de precipitado, agua, papel secante. Se introduce un trozo de nieve carbónica en un vaso de precipitados que contiene agua con un poco de jabón. Inmediatamente se forman burbujas que salen del vaso y que conviene recoger con el papel secante porque se deslizan hacia abajo. Cuestión: ¿Qué gas contienen las pompas de jabón? ¿Porqué caen en lugar de elevarse? Experiencia 6. Congelación espontánea del agua. Material: nieve carbónica, vaso de precipitado, agua, cuchara de metal. Si tenemos el hielo seco en un vaso de precipitados y lo tocamos con una cuchara de metal que contiene agua esta se congelará de manera instantánea. Experiencia 7. Preparación de mezcla refrigerante. Material: nieve carbónica, vaso de precipitado, acetona, termómetro de baja temperatura. Dato: Punto de fusión de la acetona = -95o C A un vaso de precipitados con un poco de acetona se añade un poco de nieve carbónica(OJO, NO AL REVÉS) y se observa con el termómetro como va bajando la temperatura. Añadir más hielo seco si es necesario. Cuestión: ¿Qué temperatura mínima podemos alcanzar si seguimos echando hielo seco? Experimentos con CO2 sólido 5 / 8
- 6. Física y Química IES Valadares Curso 2020-21 Experiencia 8: Carácter ácido del CO2 en agua Material: nieve carbónica, vaso de precipitado, agua, azul de bromotimol, disolución de hidróxido sódico 2N. En un vaso de precipitado se agrega agua, una pizca de azul de bromotimol (hasta coloración azul patente) y dos o tres gotas de disolución de hidróxido sódico de manera que el sistema mantenga un pH básico (comprobar con papel indicador). A continuación, se coge un poco de nieve carbónica y se introduce en el interior del recipiente, sobre la disolución. Se agita vigorosamente, observándose burbujas de dióxido de carbono y una neblina blanca. Tras unos momentos agitando, la disolución se vuelve amarilla (comprobar el pH con papel indicador). El color azul original se restablece al añadir nuevamente unas gotas de la disolución de hidróxido sódico. Mientras siga quedando CO2 sólido sobre la superficie, puede repetirse el proceso observando nuevamente el paso de la disolución a amarillo. Experimentos con CO2 sólido 6 / 8
- 7. Física y Química IES Valadares Curso 2020-21 Solucionario Experiencia 1 El hielo seco se desliza casi sin rozamiento ya que se forma un "colchón de gas" entre el bloque de hielo y la mesa. Experiencia 2 Al aumentar la temperatura, se forma CO2 gaseoso, que se disuelve relativamente poco en el agua (1,5 g/litro de agua a 25 °C y 1 atm) y se desprende en forma de grandes burbujas. Los "humos" blancos son en realidad una niebla de finas gotitas de agua arrastradas por el CO2 y se deslizan por el exterior del recipiente hacia abajo porque el CO2 es más denso que el aire (1,5 veces, aproximadamente). Tiene lugar la sublimación del CO2 , la solidificación de la parte de abajo del agua porque baja la temperatura del agua. Por otra parte, el efecto producido por el hielo seco en el agua representa el mismo fenómeno a menor escala que el de las nubes. A medida que el dióxido de carbono se sublima, el dióxido de carbono en fase gaseosa todavía está bastante frío. Por eso el agua en el aire se condensa en el gas frío de dióxido de carbono a medida que se eleva por encima del agua. A bajas temperaturas el agua se condensará del aire en gotas muy pequeñas de agua formando esa niebla. Experiencia 3 La llama de una vela, como toda combustión, se alimenta de oxígeno. Si se deja salir con cuidado el dióxido de carbono gaseoso desde un recipiente contenedor, y se vierte sobre el vaso que contiene las velas, este fluirá rápidamente al fondo del vaso y desplazará al oxígeno al ser más denso que este. Al no ser combustible (no arde), ni comburente (no deja arder), apagará la llama. Experiencia 4 En el caso del globo con nieve carbónica en su interior, el volumen aumenta puesto que está aumentando la cantidad de gas en su interior según sublima el CO2. No aparecen gotas porque el CO2 no pasa por estado líquido y el globo no flota en el aire porque el CO2 que hay en su interior es más denso que el aire. Experimentos con CO2 sólido 7 / 8
- 8. Física y Química IES Valadares Curso 2020-21 Experiencia 5 Las pompas no tienen aire en su interior sino CO2 por eso caen en lugar de elevarse. Experiencia 6 El agua en contacto con el hielo seco se congelará al instante por la gran diferencia de temperatura. En igualdad de peso, el hielo seco es capaz de refrigerar un 170% más que el hielo convencional. Por eso es capaz de refrigerar a mayor velocidad. Experiencia 7 Podremos alcanzar -78o C que es la temperatura de fusión del CO2 Experiencia 8 El CO2 se disuelve en agua y su presencia en esta da lugar a una reacción de hidrólisis en la que se generan protones: Al añadir unas gotas de hidróxido potásico a la disolución de azul de bromotimol, el agua resultante es básica y la disolución presenta un color azul intenso. La presencia de CO2 en el medio libera protones, neutralizando los grupos hidroxilo de la base, hasta que la disolución se vuelve finalmente ácida y su color pasa a amarillo. El color azul original se restablece al añadir unas gotas disolución de hidróxido de sodio ya que los grupos hidroxilo neutralizan ahora a los protones y el pH aumenta. Sin embargo, la disolución se volverá de color amarillo mientras la nieve carbónica esté presente. Experimentos con CO2 sólido 8 / 8