Presentación1
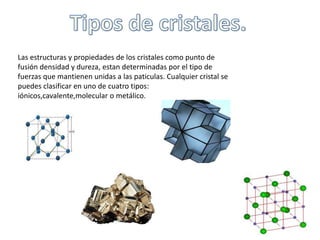
- 1. Las estructuras y propiedades de los cristales como punto de fusión densidad y dureza, estan determinadas por el tipo de fuerzas que mantienen unidas a las paticulas. Cualquier cristal se puedes clasificar en uno de cuatro tipos: iónicos,cavalente,molecular o metálico.
- 2. Cristales covalentes. Los atomos de los cristales covalentes se matienen unidos enuna red tridimensional unicamente por enlaces covalentes. Los dos alótropos del carbono, el diamante t el grafito, son ejemplo bien conocidos. En el diamante, cas atomo de carbono presenta hobridación. Esta enlazado a otros cuatro atomos. Los enlaces covalentes fuertes en tres dimensiones contirbuyen a la dureza particular del diamante y a su elevado punto de fusion.
- 3. Cristales Moleculares. En un cristal molecular, los puntos reticulares estan ocupados por moleculas que se mantienen unidas por fuerzas de van der Waals y de puentes de hidrogeno. El dioxido de azufre( SO2) solido es un ejemplo de un cristal molecular, en el que la fuerza de atraccion predominante es una interaccion dipolo-dipolo. Los puentes de hidrogeno intermoleculares son los que mantienen la red tridimensional del hielo.
- 4. Cristales Métalicos. Los cristles metalicos por lo regular tienen una estructura cúbica centrada en el cuerpo o centrada en la caras; tambien pueden ser hexagonales de empaquetamiento compacto. Por consigueinte, los elementos metalicos suelen ser muy densos. Los enlaces en los critales de metales son diferentes de los de otros tipos de cristales. La movilidad de los electrones deslocalizados hace que los metales sean buenos conductores de calor y electricidad.