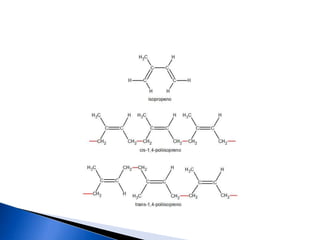
Los materiales no cristalinos carecen de un arreglo tridimensional y presentan un orden de corto alcance, permitiendo que se solidifiquen de manera gradual sin un punto de fusión definido. Su estructura puede ser afectada por factores como la longitud de las cadenas moleculares y la presencia de grupos laterales grandes, lo que explica su naturaleza amorfa y características como la transparencia. Ejemplos incluyen polímeros como el polietileno y vidrios como la sílice, que pueden formar estructuras no cristalinas bajo ciertas condiciones de enfriamiento.