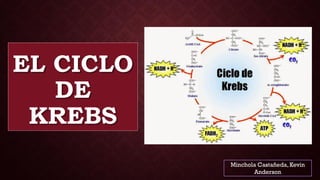
Ciclo de Krebs
- 2. CICLO DE KREBS Secuencia de reacciones Oxida el residuo acetil de la acetil-CoA a CO2 Reduce las coenzimas que se reoxidan a través de la cadena respiratoria. Vía final común OXIDACIÓN Carbohidratos Lípidos Proteínas El ciclo de Krebs consta de 8 pasos
- 3. 1. Formación del citrato El CoA-SH liberado se recicla Enzima: Citrato sintasa Forma un enlace carbono- carbono entre el carbono metílico del acetil-CoA y el carbono carbonílico del oxaloacetato
- 4. 2. Formación de isocitrato vía cis-aconitato Enzima: Aconitasa Dos pasos Deshidratación a cis-aconitato Rehidratación a isocitrato El cis-aconitato normalmente no se separa del sitio activo Inhibe la aconitasa y hace que el citrato se acumule FLUORACETATO
- 5. 3. Oxidación del isocitrato a α-cetoglutarato Enzima: Isocitrato deshidrogenasa Requiere de iones Mg2+ o Mn2+ 3 isoenzimas Usa NAD+: Mitocondria Usa NADP+: Citosol Usa NADP+: Mitocondria
- 6. 4. Oxidación del α-cetoglutarato a succinil-CoA Enzima: Complejo α-cetoglutarato deshidrogenasa 5 cofactores Tiamina difosfato (TPP) NAD+ Lipoato FAD CoA Arsenito Inhibe la reacción y provoca que el alfacetoglutarato se acumule
- 7. 5. Conversión del succinil-CoA a succinato Enzima: Succinato tiocinasa Único ejemplo de fosforilación a nivel de sustrato en el ciclo 2 isoenzimas Específica para el GDP Específica para el ADP Hígado y riñón Tejidos no glucogénicos solo tienen una isoenzima que fosforila ADP
- 8. 6. Oxidación de succinato a fumarato Enzima: Succinato deshidrogenasa Enzima unida a la superficie interna de la membrana mitocondrial interna Malonato Fuerte inhibidor competitivo de la succinato deshidrogenasa
- 9. 7. Hidratación de fumarato a malato Enzima: Fumarasa Cataliza la adición de aguda a través del doble enlace del fumarato El estado de transición de esta reacción es un carbanión
- 10. 8. Oxidación del malato a oxalacetato Enzima: Malato deshidrogenasa En equilibrio, esta reacción favorece al malato El flujo neto es hacia es oxalacetato debido a su constante uso
- 12. GLUCOGÉNESIS Síntesis de glucógeno 3 REACCIONES 1. Síntesis de glucosa-1-fosfato Enzima: Fosfoglucomutasa Contiene un grupo fosfato unido a un residuo de serina reactivo
- 13. 2. Síntesis de UDP-glucosa Enzima: UDP-glucosa pirofosforilasa El UDP-glucosa es más reactivo que la glucosa y se mantiene de forma más segura en el sitio activo de las enzimas glucosiltransferasas El pirofosfato resultante es hidrolizado irreversiblemente por la pirofosforilasa
- 14. 3. Síntesis de glucógeno a través de UDP-glucosa Enzima: Glucógeno sintasa Se requiere de un tetrasacárido preexistente Glucogenina (Proteína cebadora) Su residuo de tirosina se une a un residuo de glucosilo del tetrasacárido preexistenteCrea enlaces α(1,4)
- 15. Enzima: amilo- α(1,4→1,6)-glucosil transferasa (enzima ramificante) Extiende la cadena de glucógeno junto a la glucógeno sintasa
- 16. GLUCOGENÓLISIS 1. Eliminación de la glucosa de los extremos no reductores del glucógeno. 2. Hidrólisis de los enlaces glucosídicos α(1,6) en los puntos de ramificación del glucógeno. Degradación de glucógeno Enzima: Glucógeno fosforilasa Utiliza fosfato inorgánico para romper los enlaces α(1,4) Enzima: Amilo-α(1,6)- glucosidasa (Enzima desramificante) eliminar los puntos de ramificación α(1,6)
- 18. Enfermedades hereditarias poco frecuentes del metabolismo del glucógenoGLUCOGENOSIS Presentan manifestaciones clínicas diversas, según el tejido más afectado Sin embargo Son los órganos que con mayor frecuencia e intensidad están afectados por las glucogenosis Hígado Músculo Autosómicas recesivas Alteración del depósito de glucógeno
- 19. 2. Glucogenosis tipo I 1. Glucogenosis tipo 0 8. Glucogenosis tipo VII 3. Glucogenosis tipo II 4. Glucogenosis tipo III 5. Glucogenosis tipo IV 6. Glucogenosis tipo V 7. Glucogenosis tipo VI 9. Glucogenosis tipo IX ↓Glucógeno sintasa ↓Glucosa-6-fosfatasa ↓Glucosa-6-fosfato translocasa ↓Enzima desrramificadora ↓Enzima ramificadora ↓Fosforilasa muscular ↓Fosforilasa hepática ↓Fosfofructocinasa muscular ↓Fosforilasa cinasa ↓α-glucosidasa ácida
- 20. REFERENCIAS BIBLIOGRÁFICAS • David L. Nelson; Michael M.Cox. Lehninger Principios de bioquímica. Omega. 5° Edición; 2009 • Murray R, Bender D, Botham K, Kennelly P, Rodwell V, Weil P. Harper Bioquímica Ilustrada. Mc Graw Hill. 31° Edición; 2018 • Baynes J, Dominiczak M. Bioquímica Médica. 4° Edición, Elsevier, España: 2015 • Labrune P., Trioche Eberschweiler P., Mollet Boudjemline A., Hubert Buron A., Gajdos V. Glycogénoses. EMC (Elsevier Masson SAS, Paris), Pédiatrie, 4-059-L-10, 2010
