RELACIONES HÍDRICAS.pptx
•Descargar como PPTX, PDF•
0 recomendaciones•1 vista
relaciones hídricas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
Similar a RELACIONES HÍDRICAS.pptx
Similar a RELACIONES HÍDRICAS.pptx (7)
Último
Último (17)
LINEAMIENTOS DE PRACTICA PECUARIA PARA EL DESARROLLO LOCAL DE LA GANDERIA BOV...

LINEAMIENTOS DE PRACTICA PECUARIA PARA EL DESARROLLO LOCAL DE LA GANDERIA BOV...
PERIODO EMBRIONARIO - El período embrionario es una etapa crítica en el desar...

PERIODO EMBRIONARIO - El período embrionario es una etapa crítica en el desar...
Murray Schafer, R. - El paisaje sonoro y la afinación del mundo [ocr] [2013].pdf![Murray Schafer, R. - El paisaje sonoro y la afinación del mundo [ocr] [2013].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Murray Schafer, R. - El paisaje sonoro y la afinación del mundo [ocr] [2013].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Murray Schafer, R. - El paisaje sonoro y la afinación del mundo [ocr] [2013].pdf
Husserl, Edmund. - Lecciones de fenomenología de la conciencia interna [ocr] ...![Husserl, Edmund. - Lecciones de fenomenología de la conciencia interna [ocr] ...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Husserl, Edmund. - Lecciones de fenomenología de la conciencia interna [ocr] ...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Husserl, Edmund. - Lecciones de fenomenología de la conciencia interna [ocr] ...
Sapiro, Gisèle. - La sociología de la literatura [ocr] [2016].pdf![Sapiro, Gisèle. - La sociología de la literatura [ocr] [2016].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Sapiro, Gisèle. - La sociología de la literatura [ocr] [2016].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Sapiro, Gisèle. - La sociología de la literatura [ocr] [2016].pdf
Dogliani, Patrizia. - El fascismo de los italianos. Una historia social [2017...

Dogliani, Patrizia. - El fascismo de los italianos. Una historia social [2017...
Marzal, Manuel M. - Historia de la antropología. Vol. II. Antropología Cultur...

Marzal, Manuel M. - Historia de la antropología. Vol. II. Antropología Cultur...
Control prenatal y posnatal de la mujer embarazada

Control prenatal y posnatal de la mujer embarazada
Marzal, Manuel M. - Historia de la antropología. Vol. I. Antropología Indigen...

Marzal, Manuel M. - Historia de la antropología. Vol. I. Antropología Indigen...
Sagredo B. R. - Historia mínima de Chile [2014].pdf![Sagredo B. R. - Historia mínima de Chile [2014].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Sagredo B. R. - Historia mínima de Chile [2014].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Sagredo B. R. - Historia mínima de Chile [2014].pdf
Marzal, Manuel M. - Tierra encantada [pdf hasta p. 131 - incompleto] [ocr] [2...![Marzal, Manuel M. - Tierra encantada [pdf hasta p. 131 - incompleto] [ocr] [2...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Marzal, Manuel M. - Tierra encantada [pdf hasta p. 131 - incompleto] [ocr] [2...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Marzal, Manuel M. - Tierra encantada [pdf hasta p. 131 - incompleto] [ocr] [2...
RELACIONES HÍDRICAS.pptx
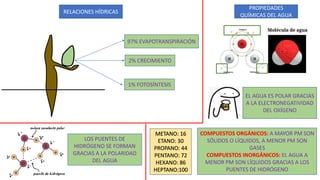
- 1. RELACIONES HÍDRICAS 97% EVAPOTRANSPIRACIÓN 2% CRECIMIENTO 1% FOTOSÍNTESIS PROPIEDADES QUÍMICAS DEL AGUA EL AGUA ES POLAR GRACIAS A LA ELECTRONEGATIVIDAD DEL OXÍGENO LOS PUENTES DE HIDRÓGENO SE FORMAN GRACIAS A LA POLARIDAD DEL AGUA METANO: 16 ETANO: 30 PROPANO: 44 PENTANO: 72 HEXANO: 86 HEPTANO:100 COMPUESTOS ORGÁNICOS: A MAYOR PM SON SÓLIDOS O LÍQUIDOS, A MENOR PM SON GASES COMPUESTOS INORGÁNICOS: EL AGUA A MENOR PM SON LÍQUIDOS GRACIAS A LOS PUENTES DE HIDRÓGENO
- 2. PROPIEDADES FÍSICAS DEL AGUA CALOR ESPECÍFICO: PARA ELEVAR LA T EN UN GRADO CENTRÍGRADO REQUIERE UNA CALORÍA 100 G DE AGUA ---- 100 CAL TEMP: 1 C 100 G DE AGUA ---- 5 CAL TEMP: 20 C CALOR LATENTE DE VAPORIZACIÓN: EL AGUA NECESITA 44 KJ/MOL PARA SU EVAPORACIÓN. ADHESIÓN - COHESIÓN: NECESARIAS PARA LA TENSIÓN SUPERFICIAL Y LA CAPILARIDAD TENSIÓN SUPERFICIAL CAPILARIDAD ASCENSO DEL AGUA EN CONTRA DE LA GRAVEDAD GRACIAS A LAS FUERZAS DE ADHESIÓN Y COHESIÓN CONSTANTE DIELÉCTRICA: MEDIDA DE CAPACIDAD DE NEUTRALIZAR LA ATRACCIÓN ENTRE CARGAS ELÉCTRICAS