Química 9°
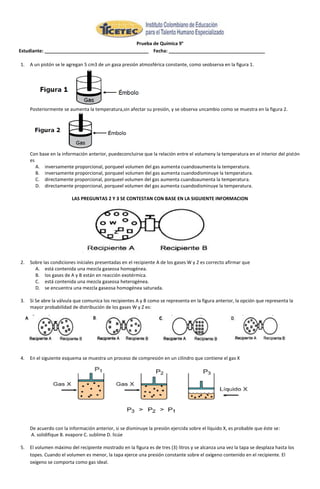
- 1. Prueba de Química 9° Estudiante: ________________________________________ Fecha: _____________________________________ 1. A un pistón se le agregan 5 cm3 de un gasa presión atmosférica constante, como seobserva en la figura 1. Posteriormente se aumenta la temperatura,sin afectar su presión, y se observa uncambio como se muestra en la figura 2. Con base en la información anterior, puedeconcluirse que la relación entre el volumeny la temperatura en el interior del pistón es A. inversamente proporcional, porqueel volumen del gas aumenta cuandoaumenta la temperatura. B. inversamente proporcional, porqueel volumen del gas aumenta cuandodisminuye la temperatura. C. directamente proporcional, porqueel volumen del gas aumenta cuandoaumenta la temperatura. D. directamente proporcional, porqueel volumen del gas aumenta cuandodisminuye la temperatura. LAS PREGUNTAS 2 Y 3 SE CONTESTAN CON BASE EN LA SIGUIENTE INFORMACION 2. Sobre las condiciones iníciales presentadas en el recipiente A de los gases W y Z es correcto afirmar que A. está contenida una mezcla gaseosa homogénea. B. los gases de A y B están en reacción exotérmica. C. está contenida una mezcla gaseosa heterogénea. D. se encuentra una mezcla gaseosa homogénea saturada. 3. Si Se abre la válvula que comunica los recipientes A y B como se representa en la figura anterior, la opción que representa la mayor probabilidad de distribución de los gases W y Z es: 4. En el siguiente esquema se muestra un proceso de compresión en un cilindro que contiene el gas X De acuerdo con la información anterior, si se disminuye la presión ejercida sobre el líquido X, es probable que éste se: A. solidifique B. evapore C. sublime D. licúe 5. El volumen máximo del recipiente mostrado en la figura es de tres (3) litros y se alcanza una vez la tapa se desplaza hasta los topes. Cuando el volumen es menor, la tapa ejerce una presión constante sobre el oxígeno contenido en el recipiente. El oxígeno se comporta como gas ideal.
- 2. Es válido afirmar que cuando el oxígeno ocupa 1,5 litros, la temperatura en el recipiente es de aproximadamente A. 600 ºK B. 300 ºK C. 450 ºK D. 150 ºK CONTESTE LAS PREGUNTAS 6 Y 7 DEACUERDO CON LA SIGUIENTE INFORMACIÓN A cuatro vasos que contienen volúmenes diferentesde agua se agrega una cantidad distintade soluto X de acuerdo con la siguiente tabla. En cada vaso se forman mezclas homogéneas 6. De acuerdo con la situación anterior, es válido afirmar que la concentración es A. mayor en el vaso 3 B. igual en los cuatro vasos C. menor en el vaso 1 D. mayor en el vaso 2 7. Si se evapora la mitad del solvente en cada uno de los vasos es muy probable que al final de la evaporación A. los cuatro vasos contengan igual masa de la sustancia X B. la concentración de las cuatro solucionessea igual C. disminuya la concentración de la solucióndel vaso dos D. aumente la masa de la sustancia X en loscuatro vasos CONTESTE LAS PREGUNTAS 8 A 10 DEACUERDO CON LA SIGUIENTE INFORMACIÓN La solubilidad indica la máxima cantidad de solutoque se disuelve en un solvente, a una temperaturadada. En la gráfica se ilustra la solubilidaddel soluto X en el solvente Y en función de latemperatura 8. La solubilidad de X en Y a 20ºC es A. 15 g de X en 100 g de Y B. 10 g de X en 100 g de Y C. 5 g de X en 100 g de Y D. 25 g de X en 100 g de Y 9. Es válido afirmar que al mezclar 15 g de X con 100 g de Y se forma una A. solución a 10ºC B. mezcla heterogénea a 20ºC C. solución a 40ºC D. mezcla heterogénea a 30ºC 10. A 40ºC una solución contiene una cantidad desconocida de X en 100 g de Y; se disminuye gradualmente la temperatura de la solución hasta 0ºC, con lo cual se obtienen 10 g de precipitado, a partir de esto es válido afirmar que la solución contenía inicialmente A. 25 g de X B. 20 g de X C. 15 g de X D. 10 g de X
