Simulacion TC
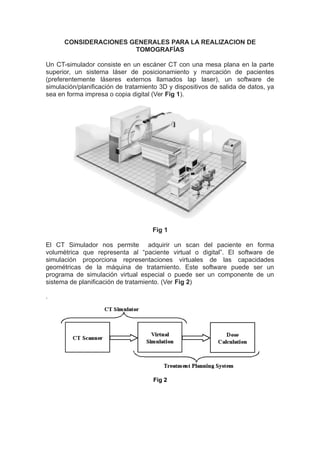
- 1. CONSIDERACIONES GENERALES PARA LA REALIZACION DE TOMOGRAFÍAS Un CT-simulador consiste en un escáner CT con una mesa plana en la parte superior, un sistema láser de posicionamiento y marcación de pacientes (preferentemente láseres externos llamados lap laser), un software de simulación/planificación de tratamiento 3D y dispositivos de salida de datos, ya sea en forma impresa o copia digital (Ver Fig 1). Fig 1 El CT Simulador nos permite adquirir un scan del paciente en forma volumétrica que representa al “paciente virtual o digital”. El software de simulación proporciona representaciones virtuales de las capacidades geométricas de la máquina de tratamiento. Este software puede ser un programa de simulación virtual especial o puede ser un componente de un sistema de planificación de tratamiento. (Ver Fig 2) . Fig 2
- 2. El diseño del proceso de simulación depende de los recursos disponibles: equipos, personal, carga de trabajo (cantidad de pacientes), la disposición física y la ubicación del sistema y sus componentes. El Proceso de CT-simulación se puede dividir en tres etapas: 1. Escaneo, posicionamiento e inmovilización del paciente 2. Planificación del tratamiento y simulación CT 3. Setup del tratamiento Escaneo, posicionamiento e inmovilización del paciente La simulación TC es, en muchos aspectos, similar a exploraciones de diagnóstico convencionales. Las principales diferencias son los requisitos para el posicionamiento e inmovilización del paciente, protocolos de exploración específicas de tratamiento, a menudo el aumento de límites de exploración, uso de contraste, la colocación marcas en la piel paciente piel, y algunas otras consideraciones especiales. Posicionamiento: dependiendo del tratamiento que se va a realizar en cada paciente, las consideraciones más importantes a la hora de elegir el posicionamiento adecuado son: Región anatómica: el médico radioterapeuta junto con el técnico de simulación deben evaluar previamente donde se encuentra anatómicamente el target y su proximidad con los órganos críticos, para determinar el mejor posicionamiento que permita acceder al mismo disminuyendo en lo posible el ingreso por los órganos a proteger. Ejemplo de esto sería si una lesión se encuentra en la parte posterior del tórax, como ser pared costal posterior, el paciente debería colocarse en decúbito ventral. Otro ejemplo podría ser el caso de irradiación de columnas dorsal o lumbar, etc. Estado general del paciente: hay que evaluar también el estado físico del paciente, para que la posición elegida sea lo más cómoda posible. Esto disminuye la posibilidad de movimientos involuntarios por cansancio, calambres, etc, durante la tomografía o el tratamiento en sí. El paciente debe tolerar la posición durante el tiempo que dure el procedimiento, en los casos de personas en estadíos avanzados, donde la movilidad está limitada, no siempre se puede elegir una posición adecuada para el target sino mas bien se considera la ubicación mas “cómoda” posible para el paciente. Equipo de tratamiento: el grupo de profesionales que realiza la simulación debe evaluar las características y limitaciones físicas de la máquina de tratamiento con la cual el paciente será tratado. Muchas veces estas limitaciones juegan un rol importante en el posicionamiento
- 3. del paciente, y en algunos casos es el factor determinante para la realización o no del tratamiento de un determinado paciente en esa máquina, por ejemplo, el peso máximo que soporta la camilla de tratamiento, el radio de giro que permita tratar un cierto diámetro de paciente, la posibilidad de girar camilla o no para ciertos tipos de tratamientos, por ejemplo de SNC, etc En todos los casos el paciente debe ser colocado en la camilla de manera alineada, por lo menos en la zona del estudio, esto permite que la posición sea reproducible durante todas las demás instancias del tratamiento. Elegir un posicionamiento adecuado es el primer eslabón de la cadena que lleva a un tratamiento exitoso, es por eso que esta etapa del proceso debe ser evaluada con el máximo cuidado posible. Inmovilización: al momento de elegir un inmovilizador hay que tener en cuenta consideraciones generales como: Que sea apropiado para cada región anatómica. Rígido. De preparación rápida y fácil. Que no altere el tratamiento (que no se interponga en el campo). Dependiendo el tipo de tratamiento, hay que considerar algunos factores que hacen una diferencia a la hora de mejorar la dosis que reciben las zonas que no se quiere irradiar. Ejemplo: Tratamientos de mama: por la anatomía de algunas pacientes, a veces ayuda colocar un plano inclinado para evitar que la mama a tratar se eleve formando un pliegue en la parte superior. En algunas pacientes, colocar el brazo contralateral al costado del cuerpo aleja la mama contralateral disminuyendo la posibilidad de irradiar con altas dosis la misma. Otras veces se puede realizar un dispositivo termoplástico que eleve la mama a modo de evitar los pliegues que se producen en las mamas pendulares (Ver foto 1 y 2)
- 4. Foto 1 y 2 En tratamientos de irradiación de mama más regián axilo supra clavicular, conviene realizar un inmovilizador personal (colchoneta de vacío) para disminuir así los posibles movimiento en la region ASCV, sobre todo si se realiza la técnica de irradiación con hemicampos. (ver foto 3, 4 y 5) Foto 3
- 5. Foto 4 Foto 5 Tratamientos de Cabeza y Cuello: Utilizar baja hombros, los hombros deben quedar lo más alineados posibles y fuera de la zona del cuello. Utilizar baja lengua con CORCHO cuando el caso requiera separar la lengua del campo de irradiación Estudiar muy bien como conviene colocar la cabeza, dependiendo la patología a irradiar, por ej.: cabeza en hiperextensión si hay que irradiar cadenas ganglionares del cuello (esto disminuye la irradiación en la mandíbula y cavidad oral) La mascara termoplástica debe cubrir de manera correcta todo el mentón desde la laringe, hasta la calota del paciente, debe quedar rígida, sin espacios vacíos entre la piel del paciente y el material, no permitir que la cabeza del paciente tenga movimientos,
- 6. (conviene sacar el molde solo cuando el material a disminuido totalmente la temperatura, para evitar así que siga contrayéndose una vez que es retirado del paciente) Foto 6 Protocolos de exploración específicas: la adquisición de los datos debe ser tal que permita tanto una buena reconstrucción de los parámetros óseos o anatómicos, así como también una buena dosimetría de los órganos críticos Dependiendo de la técnica de tratamiento a entregar, 3D, IMRT, IGRT, etc, del tamaño de la lesión, y de los márgenes de seguridad que se le da a cada estructura, se debe adquirir cortes entre dos a cinco milímetros. Por ejemplo, en casos de IGRT de próstata, donde se implantan marcadores de oro en formas de semilla que no superan una longitud de 2 mm, los cortes tomográficos deberían ser cada 1 a 1,5 mm con el fin de asegurar no perder la información de las mismas en el estudio. Para los órganos de riesgo en serie, como la médula espinal por ejemplo, solo se evalúa la dosis máxima a la que está expuesta. Sin embargo para los órganos en paralelo (pulmones, riñones, corazón, hígado, etc) se debe tener la información de todo el volumen para evaluar correctamente la relación Dosis- Volumen. Es decir, por ejemplo, si la zona a irradiar está localizada en el tórax, el estudio debe abarcar la totalidad de los pulmones ya que los valores de dosis permitidos establecidos en las tablas de referencia consideran el volumen total del órgano. Los límites del estudio entonces varían de acuerdo a la patología y zona a irradiar. Debe ser establecido por el médico antes de realizar el estudio teniendo en cuenta los factores antes mencionados. Uso de contraste y colocación marcas en la piel paciente piel: algunas patologías requieren la utilización de contraste para observar mejor la separación entre los distintos tejidos y poder marcar así los órganos de riesgos y los targets de manera más exacta. El contraste endovenoso ayuda al médico radioterapeuta a visualizar mejor la pared vesical, por ejemplo, o estructuras vasculares. Para la zona abdominal y pelviana, administrar contraste oral
- 7. permite delimitar las asas intestinales y el estomago, y lograr así una mejor delineación del target. Para los tratamientos de próstata y pelvis, se debe colocar zondas rectales que permiten delimitar el recto y ayudan a desalojar gases indeseados en el mismo, los cuales hacen que la ubicación del recto no sea reproducible durante el tratamiento en sí. Para lograr el mismo efecto en la vejiga, el estudio se debe realizar con un llenado vesical conocido. Para tratamientos de mama, se debe marcar en la piel del paciente, los límites anatómicos de la misma, esto se realiza con la exploración manual, y es el médico radioterapeuta el que debe entrenar de manera correcta al técnico del tomógrafo para hacerlo. Las marcas deben ser tales que permitan reconocer luego en los cortes tomográficos dichos limites pero que a la vez no produzcan demasiados artefactos en la imagen. También se deben marcar los límites de la cicatriz para asegurar así una correcta cobertura de la zona donde se va a realizar, en caso de ser necesario, el boost en el lecho operatorio. Para la colocación de los marcadores de posicionamiento, se requiere primero comprender qué tipo de tratamiento y en qué zona se va a realizar el estudio. Las mismas se deben elegir lo suficientemente lejos del centro de la zona a trata, para no crear confusión con los tatuajes de tratamientos, pero también lo suficientemente cerca de modo tal que permitan posicionar de igual forma todos los días la zona de tratamiento. No deben colocarse en pliegues o zonas de mucha pendiente, y tienen que ser suficientes para tener la información de los tres ejes espaciales, esto significa que con un solo tatuaje de posicionamiento no alcanza, lo ideal es que sean tres (anterior/posterior y laterales) o pueden ser solamente dos, mientras contengan la información de los ejes que permitan colocar de forma correcta al paciente en forma sagital, coronal y vertical. En los casos de simulación virtual de próstata, estos marcadores de posicionamiento solo ayudan durante la simulación a localizar luego, por medio de los láser externos, las coordenadas del isocentro (centro de próstata) y son estos últimos los que se tatúan definitivamente en la piel del paciente.
