bacterias rizosfericas
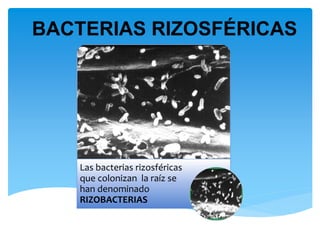
- 1. Las bacterias rizosféricas que colonizan la raíz se han denominado RIZOBACTERIAS BACTERIAS RIZOSFÉRICAS
- 3. Los microorganismos que habitan en la rizosfera liberan diferentes metabolitos entre los que están los reguladores del crecimiento vegetal tales como: etileno, ácido giberélico (AG), ácido indol ácético (AIA), ácido ábcisico y citoquininas. Otras sustancias liberadas por la actividad microbiana en la rizosfera incluyen las fitotoxinas tales como el ácido para-amimo- benzoico, ácido cumárico, ácido acético, ácido cianhídrico, ácido sulfhídrico y ácido benzoico. Además numerosas moléculas con actividad biostática y (antibióticos) son liberadas por bacterias, actinomicetos y hongos.
- 4. Pseudomonas LAS RIZOBACTERIAS QUE EJERCEN EFECTOS BENÉFICOS SOBRE EL DESARROLLO DE LAS PLANTAS SON LLAMADAS RIZOBACTERIAS PROMOTORAS DEL CRECIMIENTO VEGETAL (PGPR) Bacillus Arthrobacter Serratia Azospirillum Rhizobium Agrobacterium
- 5. Rizobacterias promotoras del crecimiento vegetal
- 6. Fijación asimbiótica de nitrógeno Efecto: Incrementar la fertilidad del suelo Realizado por bacterias de vida libre: Azoarcus, Azotobacter, Acetobacter, Alcaligenes, Azomonas, Bacillus, Beijerinckia, Clostridium, Derxia, Enterobacter.
- 7. Solubilización de fósforo. Pseudomonas Bacillus, Azospirillum, Azotobacter, rizobios. Producción de sideróforos. Efecto directo: aumenta disponibilidad del fierro. Efecto indirecto: Inhibe el crecimiento de potógenos. Pseudomonas, Bacillus, Enterobacter, Klebsiella, Burkholderia, Rizobios.
- 8. SIN INOCULAR INOCULADA Bacillus, Azospirillum, rizobios, Pseudomonas, Erwinia, Enterobacter, Klebsiella. PRODUCCIÓN DE SUBSTANCIAS FITOESTIMULANTES POR Azospirillum EN PLANTAS DE MAÍZ
- 9. Tanto las plantas como los microorganismos rizosféricos liberan sustancias que contribuyen a formar agregados entre partículas minerales y el humus. A estas sustancias tanto de origen vegetal (lectinas) como de origen microbiano (gomas, exopolisacáridos, capas mucosas y polímeros) se les conoce como aglutininas o agentes de agregación del suelo. En la rizosfera se han detectado más de 50 actividades enzimáticas que regulan los procesos biológicos en este hábitat, destacando hidrolasas, oxidoreductasas, pectinasas y DNAsas entre otras. Los factores que influyen en el efecto rizosférico incluyen las especies vegetales, el estado fenológico de la vegetación, la microbiota rizosférica, el tipo de suelo y el ambiente.
- 10. Métodos para evaluar la diversidad de PGPR Técnicas clásicas Técnicas moleculares Aislamiento de rizobacterias Selección de las posibles PGPR Demostración de la promoción del crecimiento vegetal Diferentes enfoques utilizados para evaluar la diversidad microbiana. Se utilizan técnicas dependientes de cultivo, técnicas moleculares o ambas. . Esquema para evaluar la diversidad de PGPR. Se basa en el aislamiento y caracterización de las rizobacterias con base en su actividad in vitro e in vivo.
- 12. Nódulos en chícharo Rhizobium sp SIMBIOSIS Rhizobium-LEGUMINOSA
- 13. Casuarina como cortina rompe vientos SIMBIÓSIS Frankia-PLANTAS NO LEGUMNINOSAS
- 14. Morfología microscópica de Frankia. NÓDULOS SIMBIÓSIS Frankia-PLANTAS NO LEGUMNINOSAS
- 15. (mycos) (rhiza) hongo + raíz = micorriza MICORRIZA
- 16. La micorriza tienen gran importancia debido a su papel en la captación y transferencia de nutrimentos minerales de la solución del suelo, como el fósforo, nitrógeno, cobre y zinc; a las plantas. Además, incrementan la captación de agua y protegen a las raíces del ataque de patógenos SIMBIOSIS MICORRÍCICA
- 18. Azospirillum
- 19. En el año de 1922, Beijerink describió una nueva especie bacteriana, a la cual nombró Azotobacter spirillum y posteriormente se denominó Spirillum lipoferum. Hasta 1975, Von Bulow y Döbereiner reportaron el aislamiento de cepas de Spirillum fijadoras de nitrógeno a partir de raíces de maíz, y en 1978 Tarrand y col. definieron al género Azospirillum.
- 20. Azospirillum es una bacteria aerobia no fermentativa quimioorganotrófica, Gram negativa. Son pleomorficos, con una longitud de 0.7 a 1.5 µm y presentan movilidad gracias a la presencia de un flagelo polar y varios laterales. Presenta un contenido de G+C de 69 a 71% Se han descrito cinco especies: A. brasilense, A. lipoferum, A. amazonense A. halopraeferans y A. irakense
- 21. Contienen gránulos de poli-β-hidroxibutirato, como material de reserva. Su temperatura óptima de crecimiento es entre 33 y 41ºC. A. lipoferum y A. halopraeferans requieren biotina para crecer. Crecen mejor en ácidos orgánicos como fuentes de carbono: malato, lactato, piruvato y succinato.
- 22. AISLAMIENTO *(solución alcohólica al 0.05%) K2HP4 0.1g KH2PO4 0.4g MgSO4 0.2g NaCl 0.1g CaCl2 0.02g FeCl3 0.01g Na2MoO4 0.002g Malato de sodio 5g Azul de bromotimol* 5 mL Agar 1.75g Agua destilada 1 L pH 6.8
- 24. CARACTERÍSTICA A. Brasilense A. lipoferum A. amazonense A. halopreferans Tamaño celular (µm) 1-1.2 1-1.5 0.8-1 0.7-1 Pleomorfismo en medio alcalino - + - + Color de la colonia en PDA Rosa Rosa Blanca No crece Reducción de nitratos a nitritos + + +/- + Reducción de nitritos a gas +/- +/- - + Requerimiento de biotina - + - + Utilización de glucosa - + + - Utilización de sacarosa y lactosa - - + - Utilización de α ceto-glutarato - + - + pH óptimo de crecimiento 6-7.8 5.7-6.8 5.7-6.5 6.8-8.0 Porcentaje de G-C 69-70 69-70 66-67 68.1
- 26. Especie de planta Éxito de la inoculación (%) Incremento en el rendimiento de la producción de grano (%) Maíz (A) 95 11-98 Maíz (B) 62 6-43 Cebada (A) 86 17-65 Trigo (A) 83 10-58 Sorgo (A) 62 6-43 A) Cultivo sin fertilización nitrogenada; B) Cultivo fertilizado con diferentes niveles de nitrógeno Inoculante elaborado por La Fundación Mexicana para la Investigación Agropecuaria y Forestal A.C Inoculación con una mezcla de Azospirillum brasilense, utilizando como soporte turba esterilizada.
- 27. El nitrógeno fijado por A. brasilense asociado a las raíces de las plantas se calcula entre 2 y 3 Kg de N/ha/año. Un cultivo en la agricultura intensiva requiere una fertilización que puede ser superior a 250 Kg N/ha/año. Por lo que el aporte de esta bacteria a los cultivos es muy bajo.
- 28. Se ha demostrado mediante diversas técnicas la producción de fitohormonas por cepas de Azospirillum en medios de cultivo: Acido indol acético: por cromatografía en placa Citocininas: Radioinmunoensayo Giberelinas: Cromatografía de gases y espectrometría de masas
- 29. PRODUCCIÓN DE SUBSTANCIAS FITOESTIMULANTES POR Azospirillum EN PLANTAS DE MAÍZ
