funciones de las enzimas
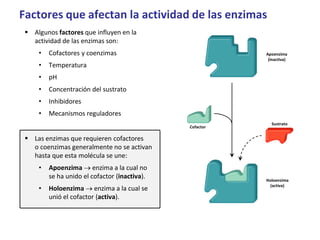
- 1. Algunos factores que influyen en la actividad de las enzimas son: • Cofactores y coenzimas • Temperatura • pH • Concentración del sustrato • Inhibidores • Mecanismos reguladores Las enzimas que requieren cofactores o coenzimas generalmente no se activan hasta que esta molécula se une: • Apoenzima → enzima a la cual no se ha unido el cofactor (inactiva). • Holoenzima → enzima a la cual se unió el cofactor (activa). Factores que afectan la actividad de las enzimas Sustrato Holoenzima (activa) Apoenzima (inactiva) Cofactor
- 2. Efecto de la temperatura El efecto de la temperatura sobre la velocidad de una reacción enzimática generalmente muestra dos etapas: 1) Aumento gradual de la velocidad de la reacción hasta alcanzar un máximo local, que se conoce como temperatura óptima. 2) Disminución progresiva de la velocidad de reacción debido a la inactivación de la enzima por desnaturalización térmica. La temperatura óptima para la mayoría de las enzimas humanas está en el rango entre los 35 y 40 oC, estas comienzan a desnaturalizarse por encima de los 40 oC. Temperatura (oC) Velocidaddereacción(v0) 1 2
- 3. Efecto del pH Los pHs extremos también pueden inactivar a la enzima por desnaturalización, por lo que el efecto del pH es similar al efecto de la temperatura sobre la velocidad de reacción. Cada enzima opera en un rango relativamente corto de valores de pH, rango en el cual sus grupos químicos se encuentran ionizados, de manera que facilitan la catálisis. • Dentro de este rango, el pH para el cual se alcanza un máximo local de velocidad se conoce como pH óptimo. • El pH óptimo para las enzimas humanas varía notablemente, alcanzando incluso valores extremos (por ejemplo: pHopt = 2 para la pepsina, una enzima gástrica). pH Velocidaddereacción(v0) Pepsina Tripsina Fosfatasa alcalina
- 4. Efecto de la concentración de sustrato El efecto de la concentración de sustrato, [S], en la velocidad de una reacción enzimática también muestra de dos etapas: 1) La velocidad de la reacción aumenta gradualmente hasta acercarse a una velocidad máxima (vmáx). 2) La velocidad se mantiene constante pues todos los centros activos de las moléculas de enzima han sido ocupados por el sustrato, se dice entonces que se presenta un comportamiento de saturación. [S] 1 2 Parámetros importantes: • vmáx • Km → valor de concentración de sustrato para el cual se ha alcanzado la mitad de la vmáx v0 vmáx ½vmáx Km Km es una medida de la afinidad de la enzima por su sustrato (a menor Km mayor afinidad).
- 5. Km baja refleja alta afinidad de la enzima por el sustrato. Km alta refleja baja afinidad de la enzima por el sustrato. [S] Enzima 2 Enzima 1
- 6. Efecto de la concentración de sustrato La relación entre v0 y [S] para una reacción enzimática fue descrita por Leonor Michaelis y Maude Menten en 1913, dando lugar a la conocida ecuación de Michaelis-Menten: La ecuación de Michaelis-Menten: • Indica que la curva de v0 vs [S] tiene forma de hipérbola, con una asíntota en vmáx. • Refleja que la velocidad de reacción es inversamente proporcional al valor de Km (afinidad de la enzima por el sustrato). La principal desventaja de este modelo es que no se cumple para todas las enzimas. A bajas concentraciones de sustrato ([S] << Km), v0 es directamente proporcional a [S]. A altas concentraciones de sustrato ([S] >> Km), v0 se mantiene constante e independiente de [S]. [S]
- 7. La inhibición enzimática ocurre cuando una molécula diferente al sustrato (denominada inhibidor) interactúa con la enzima, impidiendo el correcto funcionamiento de esta. Hay muchos tipos de inhibidores, pero los más representativos son: Inhibición enzimática Inhibidores competitivos • Tienen cierta afinidad con el centro activo (análogos estructurales del sustrato). • Compiten con el sustrato, pero la reacción no procede tras la unión. Inhibidores no competitivos • Generalmente se unen a un sitio diferente al centro activo. • La unión ocurre tras la formación del complejo ES, afectando así la ocurrencia de la reacción.
- 8. Todos los inhibidores provocan una disminución de la velocidad de la reacción enzimática (afectan la eficiencia de la enzima). No obstante, cada tipo de inhibidor afecta de manera diferente a los parámetros cinéticos. Inhibición enzimática Inhibidores competitivos • Al competir con el sustrato, disminuyen la afinidad de la enzima por este: • Aumentan el valor de Km. • No modifican la vmáx, pero la saturación se alcanza a mayor concentración de sustrato. Inhibidor competitivo Inhibidores no competitivos • Puesto que no compiten con el sustrato: • No modifican el valor de Km. • Disminuyen directamente el valor de vmáx. Inhibidor no competitivo
- 9. Inhibidores como medicamentos Más de la mitad de los medicamentos de consumo aprobado y de venta en las farmacias actuales son en realidad inhibidores enzimáticos. Inhibidor Enzima a la que inhiben Efecto Antibióticos β-lactámicos (ej. Penicilina) Enzimas de la síntesis de la pared celular bacteriana Reducción de la población de la bacteria patógena en el huésped. Antivirales análogos a guanosina (ej. Aciclovir) DNA polimerasa viral Bloquean la replicación del ADN viral y por ende, del propio virus. Estatinas (ej. Lipitor) HMG-CoA reductasa humana (síntesis de colesterol) Disminución del nivel plasmático de colesterol. Reductores de la presión sanguínea (ej. Captopril, Enalapril) Enzima convertidora de angiotensina (ACE) humana Bloquean la conversión de la angiotensina I en angiotensina II (potente vasoconstrictor). Antifolatos (ej. Metotrexato, Aminopterina) Dihidrofolato reductasa Interfieren con la división celular, por lo que puede usarse como agentes antineoplásicos o como antibióticos. Citrato de sildenafil (Viagra) Fosfodiesterasa tipo 5 (PDE5) Promueve el flujo de sangre al pene, por lo que se usa como tratamiento de disfunciones eréctiles.
- 11. cGMP (sustrato natural de la enzima PDE5) Viagra (inhibidor de la PDE5 por analogía con el sustrato)
- 12. Enzimas en el diagnóstico clínico El hallazgo de concentraciones sanguíneas elevadas para enzimas propias de los diferentes tejidos permite diagnosticar la existencia de patologías en estos tejidos. En condiciones normales: • La concentración sanguínea de las enzimas tisulares es baja. • Estas pequeñas concentraciones basales se deben al recambio celular normal. En situaciones patológicas los niveles plasmáticos de las enzimas exclusivas de los tejidos afectados suele aumentar. • Esto puede ocurrir por: ◦ La existencia de daño celular (ruptura de células) en dichos tejidos. ◦ Un alto grado de proliferación celular, usualmente asociado a formaciones tumorales. Enzimas Recambio celular ProliferaciónDaño tisular
- 13. Algunas enzimas importantes en el diagnóstico clínico Enzima Uso diagnóstico Alanina transaminasa (transaminasa pirúvica) (ALT) Hígado (perfil hepático) Aspartato transaminasa (transaminasa oxaloacética) (AST) Infarto del miocardio, hígado (en menor grado que ALT) Creatina quinasa (CK) Infarto del miocardio, músculo en general Amilasa intestinal Páncreas Lipasa intestinal Páncreas Lactato deshidrogenasa (LDH) Hemólisis Fosfatasa ácida Próstata Fosfatasa alcalina Trastornos óseos, hígado (enfermedades obstructivas)
- 14. Mecanismos reguladores La actividad de las enzimas in vivo está regulada por múltiples mecanismos, que pueden tener un efecto positivo o negativo, según las necesidades celulares. Principales mecanismos reguladores: • Clivaje proteolítico → Algunas enzimas se sintetizan como precursores inactivos (proenzimas o zimógenos), que se activan luego por el corte de uno o más segmentos de cadena. Todas las proteasas digestivas se secretan en forma de zimógenos. • Alosterismo (próximas diapositivas). • Modulación covalente (próximas diapositivas). • Regulación de la expresión (síntesis) de la enzima a nivel de la transcripción. • Degradación de la propia enzima. Proteasa Zimógeno (inactivo) Enzima activa
- 15. El alosterismo es una forma de regulación en la que una molécula endógena (conocida como modulador alostérico) se une a la enzima y modula su actividad. No todas las enzimas están sujetas a este tipo de regulación, las que lo están se conocen como enzimas alostéricas o reguladoras. Los moduladores alostéricos: • Se unen siempre a sitios específicos (sitios alostéricos), diferentes al centro activo de la enzima. • La unión media un cambio en la enzima que puede ser favorable o desfavorable. • Pueden ser positivos (si aumentan la actividad de la enzima) o negativos (si la disminuyen). • Estos no se consideran como inhibidores, pues son endógenos y actúan de manera diferente. Forman parte de la función normal de la proteína. Alosterismo Sustrato Moduladoralostérico positivo Enzima menos activa Enzima más activa
- 16. A diferencia de los inhibidores, los moduladores alostéricos modifican la manera en la que la velocidad de reacción depende de la concentración de sustrato. Para las enzimas alostéricas: • No se cumple la ecuación de Michaelis-Menten. • La curva de v0 vs [S] no tiene forma hiperbólica, sino sigmoidal (forma de S alargada). • La concentración para la cual se alcanza la mitad de la vmáx no se denota como «Km», sino como K0.5, aunque esta tiene una implicación similar en cuando a la afinidad E-S. Alosterismo Enzima con una cinética de tipo Michaelis-Menten. Enzima alostérica. [S] v0
- 17. [S] v0 MA+ MA–
- 18. La enzimas alostéricas se encuentran muchas veces ubicadas en puntos estratégicos en las vías metabólicas, regulando el flujo metabólico de acuerdo a las necesidades de la célula. La retroinhibición o inhibición feedback es una forma de regular el metabolismo, en la que los productos finales de una vía metabólica son moduladores alostéricos negativos de una enzima reguladora ubicada al principio de la vía. De esta forma se evita: • Gastar energía y compuestos intermediarios cuando hay suficiente producto final. • Degradar los intermediarios iniciales cuando hay carencia de estos, por haber sido usados en la producción del producto final. El alosterismo en el metabolismo: retroinhibición
- 19. La modulación covalente consiste en la unión covalente y temporal de grupos pequeños a la enzima. • Esta unión puede tener un efecto positivo o negativo, según la enzima. • La más común es la unión de grupos fosfato, denominada fosforilación. Sobre la fosforilación: • El grupo fosfato se une generalmente a residuos de Tyr, Ser, Thr ó His. • Este grupo es aportado por un nucleótido trifosfato (ATP, GTP). • La llevan a cabo enzimas conocidas como quinasas o cinasas. • La reacción inversa (eliminación del grupo fosfato) tiene efecto contrario en la enzima y es llevada a cabo por otras enzimas conocidas como fosfatasas. Modulación covalente Enzima inactiva Enzima activa P
- 20. Regulación hormonal El mecanismo de modulación covalente permite que la actividad de las enzimas pueda ser regulada en respuesta a estímulos extracelulares. • La señal externa se trasmite al interior de la célula mediante un sistema de transducción de señales. Un sistema de este tipo involucra: • Un primer mensajero extracelular, usualmente una hormona. • Una proteína integral de membrana, conocida como receptor. ◦ Este reconoce a la hormona y trasmite el estimulo al interior. • Un sistema efector, encargado de activar la respuesta intracelular. ◦ Este puede ser activado por un segundo mensajero intracelular (diferente a la hormona). ◦ La respuesta usualmente implica la fosforilación de múltiples proteínas intracelulares. Receptor Hormona Membrana EXT INT Sistema efector
- 21. E E E G E RECEPTORES CON ACTIVIDAD ENZIMÁTICA RECEPTORES ACOPLADOS A PROTEÍNA G RECEPTORES SIN ACTIVIDAD ENZIMÁTICA INTRÍNSECA Respuesta Respuesta Respuesta E R R R R R 2º M 2º M 2º M
- 22. Receptores con actividad enzimática Estos receptores tienen dos dominios principales: • Dominio extracelular → función receptora • Dominio intracelular → función catalítica (quinasa) La recepción de la señal por el dominio extracelular hace que se active la función enzimática del dominio intracelular y este pueda entonces trasmitirla al medio interno. El ejemplo más representativo es el del receptor de insulina. • El dominio intracelular tiene actividad tirosina quinasa (puede autofosforilarse y fosforilar a otras proteínas). Insulina E E Respuesta 2º M R R
- 24. Receptores acoplados a proteína G (GPCRs) Estos sistemas constan de tres componentes: • El receptor per se. • Una enzima de membrana que media la síntesis del segundo mensajero intracelular (por ejemplo la adenilato ciclasa, que convierte el ATP en AMP cíclico, cAMP). • Una proteína que actúa como nexo entre los dos primeros, denominada proteína G (porque puede unir GDP y GTP). Muchas hormonas y neurotransmisores funcionan mediante GPCRs, por ejemplo: • Glucagón. • Epinefrina (adrenalina). • Corticotropina (ACTH). • Dopamina. • Prostaglandinas. • Serotonina. G E R Respuesta 2º M
- 25. (…)
