SOLUCIONES QUIMICAS.pdf
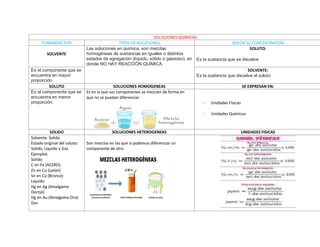
- 1. SOLUCIONES QUIMICAS FORMADAS POR TIPOS DE SOLUCIONES SEGÚN SU CONCENTRACION SOLVENTE Las soluciones en química, son mezclas homogéneas de sustancias en iguales o distintos estados de agregación (líquido, sólido o gaseoso), en donde NO HAY REACCIÓN QUÍMICA. SOLUTO: Es la sustancia que se disuelve Es el componente que se encuentra en mayor proporción SOLVENTE: Es la sustancia que disuelve al soluto SOLUTO SOLUCIONES HOMOGENEAS SE EXPRESAN EN: Es el componente que se encuentra en menor proporción. Es en la que sus componentes se mezclan de forma en que no se puedan diferenciar. - Unidades Físicas - Unidades Químicas SOLIDO SOLUCIONES HETEROGENEAS UNIDADES FISICAS Solvente: Solido Estado original del soluto: Solido, Liquido y Gas Ejemplos Solido C en Fe (ACERO) Zn en Cu (Latón) Sn en Cu (Bronce) Liquido Hg en Ag (Amalgama Dental) Hg en Au (Amalgama Oro) Gas Son mezclas en las que si podemos diferenciar un componente de otro
- 2. H2 en Pd (Oclusión de H2 en Pd) H2 en Pt (Oclusión de H2 en Pt) LIQUIDO SOLUCIONES ELECTROLITICAS % MASA A MASA Solvente: Liquido Estado Original del soluto: Solido, líquido y Gas Ejemplos Solido Nacl en Agua (Salmuera) Son Soluciones que, si pueden transmitir electricidad, se las puede llamar también iónicas. Se define como la masa de soluto presente en 100 gramos de disolución. Liquido CH3COOH en H2O(VINAGRE) C2H5OH en H2O(AGUARDIENTE) SOLUCIONES NO ELECTROLITICAS % PESO Y VOLUMEN Tiene una escasa posibilidad de transmitir electricidad y se caracterizan, principalmente, porque el soluto se disgrega casi hasta su estado molecular. Es la relación en porcentaje entre el peso del soluto y el volumen de la solución. (g de soluto/mL de solución) *100. % VOLUMEN A VOLUMEN
- 3. GAS CO2 en H20(AGUA GASIFICADA) O2 en H20 DE RIO Y LAGO. Es una medida de la concentración que indica el volumen de soluto por cada 100 unidades de volumen de la solución: % (V/V) = Volumen de soluto · 100 Volumen de la disolució GASEOSO SOLUCIONES SATURADAS UNIDADES QUMICAS Solvente: Gas Estado Original Del Soluto: Solido, Liquido y Gas Ejemplos Solido 12 en AIRE C10 H8(NAFTALINA) EN AIRE Liquido H2O en AIRE (AIRE HUMEDO) GASOLINA en AIRE Son aquellas en donde hay mayor cantidad de soluto disuelto, ósea esta al limite en cuanto a cantidad de soluto en solvente MOLARIDAD: Se define como la cantidad de soluto (expresada en moles) por litro de disolución Moles de soluto/L de solución. SOLUCIONES INSATURADAS MOLALIDAD: Conocidas como diluidas, Se tiene una pequeña cantidad de soluto en el solvente; por lo tanto, este es casi imperceptible. Este término alude a la cantidad de moles de soluto que hay en cada kilogramo de solvente.
- 4. Moles de soluto/kg de solvente. SOLUCIONES CONCENTRADAS O NO SATURADAS FRACCION MOLAR: Gas CH3HS en C3H8(GAS DOMESTICO) 02 en N2(AIRE ARTIFICIAL) Es una solución en donde el porcentaje de soluto se acerca al establecido por la solubilidad. Se define como el cociente entre los moles de soluto y el total, de moles de la disolución, que se calcula sumando los moles de soluto(s) y de solvente n de soluto/n de solución. PARTES POR MILLON (ppm) es una unidad de medida de concentración. Se refiere a la cantidad de unidades de la sustancia (agente, etc) que hay por cada millón de unidades del conjunto.