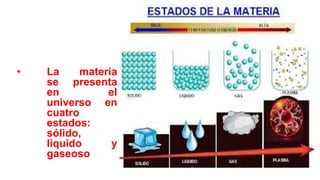
Estados de la materia y cambios
- 1. • La materia se presenta en el universo en cuatro estados: sólido, líquido y gaseoso
- 2. Compresividad capacidad de las moléculas de una sustancia para dejarse comprimir, es decir disminuir su volumen al someterlos a una presión o compresión Difusión paso o expansión de moléculas de un medio a otro: el humo se difunde en el aire, la tinta se difunde en el agua. La difusión de los sólidos ocurre lentamente a temperatura ambiente Energía cinética energía que posee un cuerpo de acuerdo a su movimiento. A mayor energía cinética, mayor distancia y menor fuerza de cohesión entre los átomos y moléculas Energía potencial energía almacenada en un sistema o en una sustancia de acuerdo a su composición. A mayor energía potencial, menor distancia y mayor fuerza de cohesión entre átomos y moléculas
- 3. • ESTADO SÓLIDO – CARACTERÍSTICAS • Forma y volumen constante, a temperatura ambiente • Espacio intermolecular mínimo (menor que en los líquidos y gases) • Fuerza de cohesión molecular mayor que la fuerza de repulsión molecular • Son prácticamente incompresibles (casi imposibles comprimirlos) • Se difunden muy lentamente (a menor velocidad que los líquidos y gases) • Al aumentar la temperatura sufren dilatación térmica
- 4. • ESTADO LÍQUIDO - CARACTERÍSTICAS • Volumen constante, forma variable (toman la forma del recipiente que los contiene) • Espacio intermolecular mayor que en los sólidos, pero menor que en los gases • Fuerza de cohesión molecular en equilibrio con la repulsión molecular • Son incompresibles • Se difunden, pero a menor velocidad que los gases • Fluidez o movilidad, sus moléculas pueden resbalar unas sobre otras sin mayor dificultad, por lo cual se pueden vaciar de un recipiente a otro
- 5. • ESTADO GASEOSO - CARACTERÍSTICAS • Tienen forma y volumen variable • El espacio intermolecular es mayor que en líquidos y sólidos • Fuerza de repulsión mayor que la de cohesión molecular (según la teoría cinética no existen fuerza de atracción molecular entre las moléculas de los gases) • Son muy compresibles, debido al gran espacio que separa las moléculas de los gases • Se difunden rápidamente y con gran facilidad (tienden a ocupar el mayor espacio posible) • Son muy elásticos
- 6. ESTADO DE PLASMA – CARACTERÍSTICAS • Forma y volumen indefinidos • Puede ser natural y artificial • Es un gas ionizado (contiene iones positivos y negativos) con igual número de cargas eléctricas libres positivas y negativas • Es buen conductor eléctrico y sus partícula responden a la interacción electromagnética; la conductividad de un plasma puede ser tratada como infinita • Es el cuarto estado de la materia más abundante, se asocia con las estrellas, nebulosas y el sol • Todos los plasman emiten luz y casi todo lo que emite luz es plasma • Fue identificado por primera vez por sir William Crookes (1879). Irving Langmuir y sus colegas (1920) denomino plasma a un gas ionizado
- 8. • El plasma no es un estado frecuente en la cotidianidad. Puede obtenerse mediante un proceso de ionización de los gases (tan simple a veces como calentarlos para hacer que sus partículas vibren más velozmente). También se puede obtener por magnetización o por aplicación de electricidad, además de otros procesos artificiales. • Se puede hacer a un plasma retornar a un estado gaseoso mediante un proceso cualquiera de des ionización, por ejemplo, retirar calor a la sustancia y permitir a sus partículas recuperar así sus electrones perdidos o ganados, dando estabilidad y volviendo a ser un gas des ionizado. Existen dos tipos de plasmas: • Plasma frío. Es el plasma en el cual la temperatura de los electrones es superior a la de las partículas más pesadas, como los iones. Este tipo de plasma es el menos dañino para los seres vivos, pues no causa quemaduras. • Plasma caliente. Es el plasma cuyos átomos ionizados se calientan enormemente debido a que están chocando continuamente, lo que genera luz y calor y, por lo tanto, podría ser peligroso para los seres vivos.
- 9. Formas comunes de plasma Producidos artificialmente Plasmas terrestres Plasmas espaciales y astrofísicos •En los televisores o monitores con pantalla de plasma. •En el interior de los tubos fluorescentes (iluminación de bajo consumo). •En soldaduras de arco eléctrico bajo protección por gas (TIG, MIG/MAG, etc.). •Materia expulsada para la propulsión de cohetes. •La región que rodea al escudo térmico de una nave espacial durante su entrada en la atmósfera. •El interior de los reactores de fusión. •Las descargas eléctricas de uso industrial. •Las bolas de plasma. •Los rayos durante una tormenta. •El Fuego de San Telmo. •La ionosfera. •Las auroras polares. •Algunas llamas. •El viento polar, una fuente de plasma. •El Sol y otras estrellas (Plasmas calentados por fusión nuclear). •Los vientos solares. •El medio interplanetario (la materia entre los planetas del Sistema Solar), el medio interestelar (la materia entre las estrellas) y el medio intergaláctico (la materia entre las galaxias). •Los discos de acrecimiento. •Las nebulosas intergalácticas. •Ambiplasma
- 10. CAMBIOS DE ESTADO DE LA MATERIA Los estados de la materia no son permanentes, cambian cuando se modifican las condiciones de temperatura o presión. Un cambio de estado es un proceso en el que una sustancia pasa de un estado físico a otro; por ejemplo, de sólido a líquido. Características de los cambios de estado • Son reversibles, es decir puede producirse tanto en un sentido como el opuesto. Cuando el oro se calienta a 1063 °C, se convierte en líquido. Se dice que se ha producido un cambio de estado. Así se puede echar en moldes que tengan diversas formas. Luego, si se deja enfriar, se convierte de nuevo en oro sólido • La temperatura permanece constante mientras dura el cambio de estado • La masa se conserva en el proceso. Es decir, si tenemos 1 kg de hielo que se convierte en agua líquida, habrá al final 1 kg de agua. Sin embargo, el volumen no siempre se conserva. En el caso del hielo, su volumen es mayor que el del agua líquida. Esto implica que la densidad del hielo es menor que la del agua líquida • Durante el proceso, o bien se absorbe calor o bien se cede calor. Para que el hielo se convierta en agua líquida hay que aplicarle calor. Por el contrario, cuando el agua líquida se convierta en hielo, cede calor
- 11. • Los cambios de estado pueden ser: progresivos cuando se dan por absorción de calor como la fusión, la vaporización y la sublimación progresiva y regresivos por liberación de calor, como la condensación, la solidificación y la sublimación regresiva Cambios progresivos: absorción de calor Cambios regresivos: liberación de calor