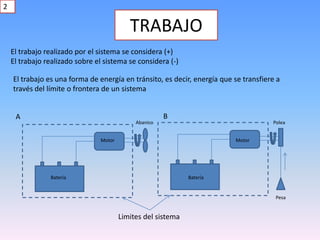
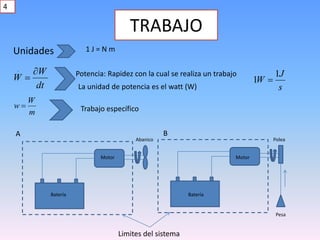
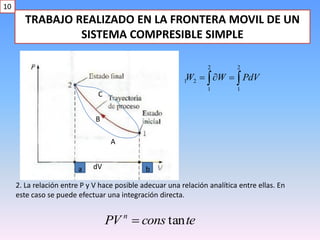
Este documento describe la diferencia entre trabajo y calor. Explica que el trabajo es una forma de energía en tránsito que se transfiere a través de los límites de un sistema debido a una fuerza que actúa a lo largo de una distancia, mientras que el calor se transfiere debido a una diferencia de temperaturas entre sistemas. También presenta expresiones matemáticas para calcular el trabajo en diferentes procesos termodinámicos como sistemas compresibles, alambres elongados y sistemas eléctricos.