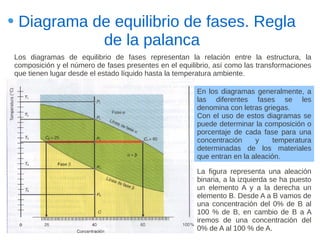
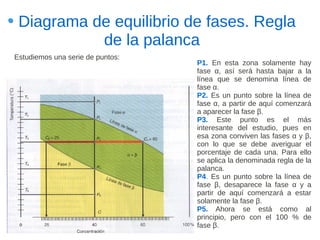
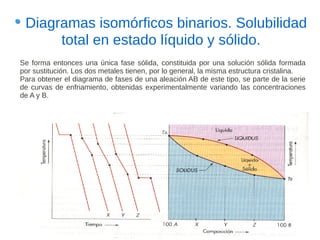
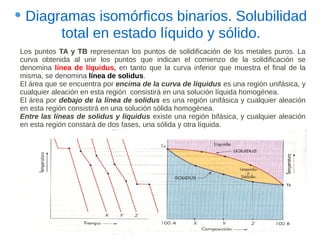
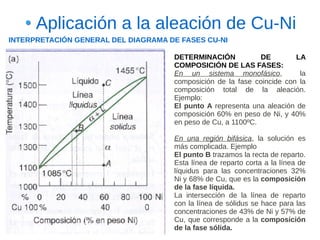
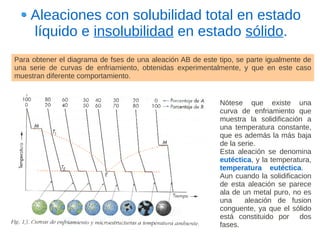
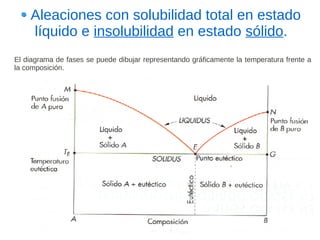
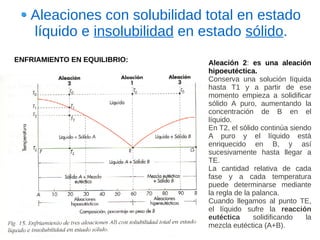
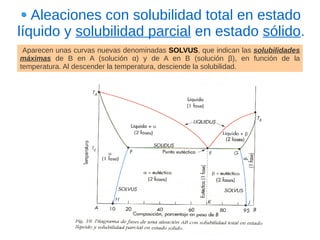
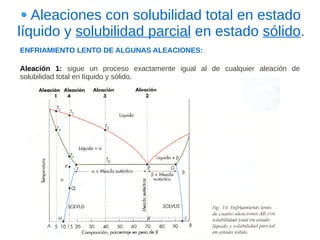
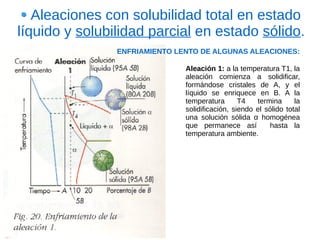
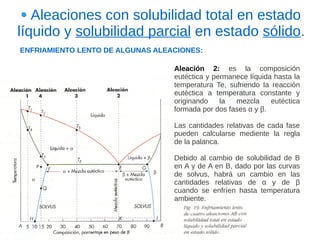
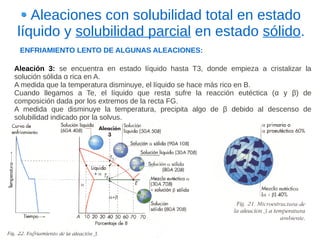
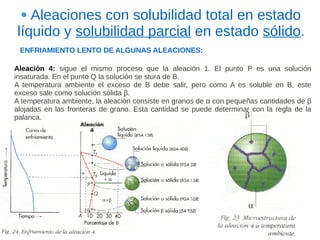
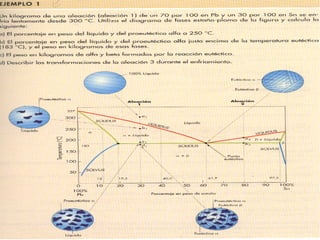
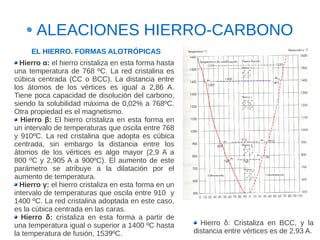
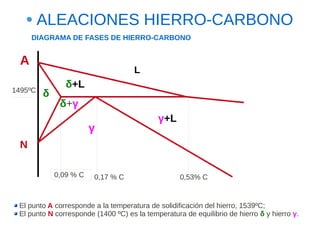
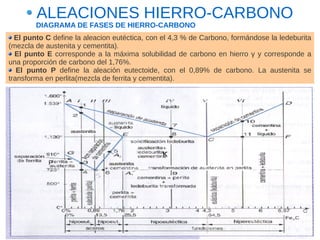
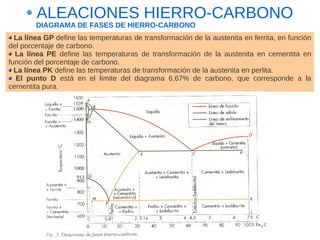
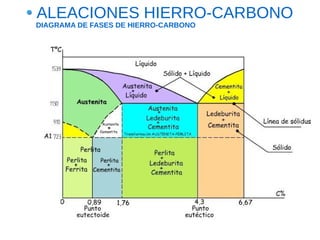
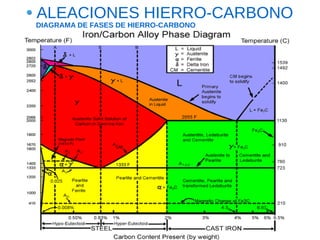
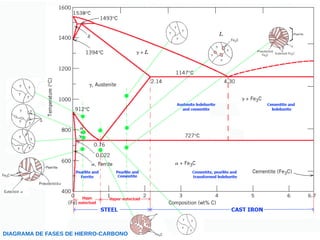
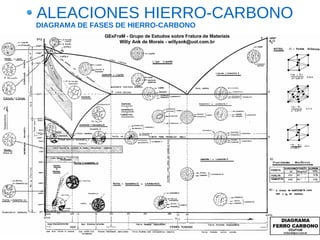
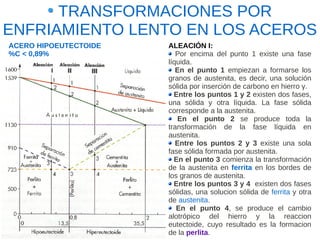
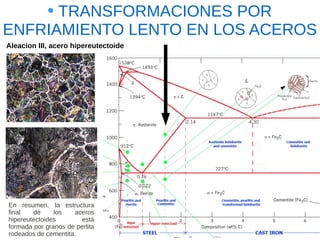
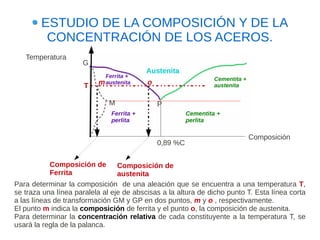
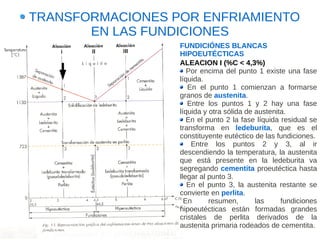
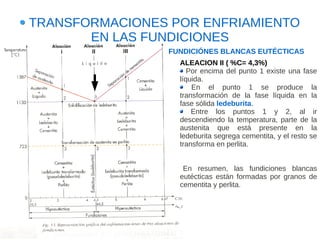
Este documento describe las aleaciones y sus diagramas de equilibrio. Explica que una aleación es la unión de dos o más elementos químicos, al menos uno de ellos metálico. Describe los tipos de estructuras cristalinas que pueden formar las aleaciones y los procesos de solidificación. También resume la regla de las fases de Gibbs y cómo se pueden usar los diagramas de equilibrio de fases para determinar las fases presentes en una aleación a diferentes temperaturas y concentraciones.