Biomembranas y biofilms.pptx
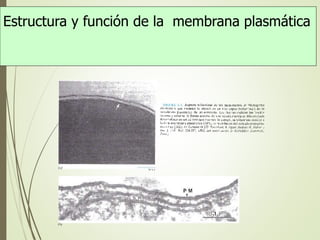
- 1. Estructura y función de la membrana plasmática
- 2. Resumen de las funciones Compartimentalización Sitios para actividades bioquímicas Provisión de una barrera de permeabilidad selectiva Transporte de solutos Respuesta a señales externas Interaccion celular Transducción de energía
- 4. Fluidez de la membrana
- 5. Capitulo 4.2 HISTORIA 1890 Ernst Overton: Solubilidad 1925 Gorter y Grendel: Bicapa lipídica 1935 Davson y Danielli: Proteínas !972 Singer y Nicolson: Mosaico fluído
- 9. A. Membrana plasmática: LÍPIDOS
- 11. C. Membrana plasmática: COLESTEROL • El colesterol amortigua la fluidez de la MP (= menos deformable) • Disminuye la permeabilidad de la MP al agua
- 16. Receptores que se unen a la superficie de la membrana Transportadores Transferentes de electrones en procesos de fotosíntesis y respiración • Brindan soporte mecánico • Enzimas especializadas • Transmiten señales
- 21. BIOFILM
- 22. Biofilms Forma de crecimiento de bacterias comunidad de bacterias adheridas a una superficie sólida e inmersa en un medio (Costerton 1987)
- 23. Desarrollo del Biofilm Biofilm Célula planctonica Bacterias desarrollan estructuras de superficie favorecen la adhesión de las mismas a una superficie sólida, tales como fimbrias y fibrillas. colonizadores primarios como Actinomyces naeslundii y Streptococcus salivarius Por otro biofilm células sueltas desprendidas de un biofilm o de partes del propio biofilm (Haffajee 2000)
- 24. Naturaleza de los biofilms Protección del biofilm a la especie colonizadora frente a mecanismos como factores ambientales y de defensa del huésped. facilitar el procesamiento y la ingestión de nutrientes Y la alimentación cruzada Los biofilms son capaces de llevar a cabo procesos metabólicos» y funciones sintéticas (Costerton 1987)
- 25. Estructura del biofilm micro colonias de células bacterianas 15/20% Presentan canales de agua permiten el paso de los nutrientes y de otros agentes a través del biofilm Actúan como un sistema «circulatorio» (Haffajee 2000)
- 26. El ciclo vital 1.Adhesión 2. Crecimiento 3. Separación o desprendimiento. 5 Fases
- 27. Fase 1 – Fijación inicial Esta fase es reversible Fase 2 – Fijación irreversible Las células que encontramos en la fase 1, quedan totalmente unidas y se protegen mediante una película de polisacáridos que les proporciona seguridad y alimento.
- 28. Fase 3 – Maduración I La multiplicación bacteriana permite que la comunidad de células crezca protegida bajo la película que las recubre. Fase 4 – Maduración II Con el crecimiento de la comunidad, también aparecen zonas especialmente creadas para la supervivencia. Es el caso de los canales de agua que fomentan aún más ese crecimiento.
- 29. Fase 5 – Dispersión La película protectora se rompe de forma natural por el agotamiento de alimento o por la alimento o por la necesidad de colonizar nuevos lugares (se retroalimenta el proceso) retroalimenta el proceso)
- 30. Heterogeneidad fisiológica Antibióticos destruyen de forma activa las células en crecimiento afectarían la capa externa del biofilm, pero no actuarían sobre las células que permanecen en su interior Las células bacterianas dentro de los biofilms pueden producir enzimas como la betalactamasa contra los antibióticos produciendo una línea de defensa casi inexpugnable. Las células bacterianas de los biofilms también pueden producir elastasas y celulasas producen lesión en los tejidos. ciertas microcolonias son anaerobias, aunque están también compuestas por especies facultativas simples y crecen al aire libre. (Aduse-Opoku 2006)
- 31. Factores que afectan el comportamiento y desarrollo del biofilm factores hidrodinámicos transporte de compuestos y la fuerza de atrición concentración de nutrientes (Haffajee 2000)
- 32. Desinserción de las células del biofilm permitir la colonización de nuevos habitantes mediante bacterias separación de una célula simple , la separación esporádica de grandes grupos de células (muda) el cual grandes partes del biofilm se desprenden Células metabólicamente activas y son capaces de crecer una vez que se han liberado del biofilm. (Socransky 1998)
- 33. Quorum Sensing señalización en la comunicación intercelular expresión de genes para la resistencia antibiótica en densidades de células elevadas puede proporcionar protección Estimula el crecimiento de especies beneficiosas (para el biofilm) e inhibiendo el crecimiento de competidores elevada densidad de células bacterianas que crecen en biofilms favorece el intercambio de información genética entre células de la misma especie (Socransky 1998)
- 34. Adhesión bacteriana microcolonias se adhieren a una superficie sólida •bacterias poseen estructuras de superficie, como fimbrias y fibrillas, ayudan a adherirse a las superficies. Las fimbrias (pili) son apéndices proteináceos similares a un pelo, de 2-8 nm •compuesta de proteínas fimbrillinas (fimbrinas). Que transportan adhesinas. S. salivarius, S. parasanguis , S. mitis (Socransky 1998)
- 35. Coagregación de bacterias asociación de bacterias dentro de biofilms mixtos las adhesinas en bacterias de diferente género pueden reconocer los mismos receptores en otras células bacterianas. adhesión célula a célula especie se coagregan con múltiples especies diferentes, y se unen a la película salival con dominio en biofilms dentales más complejos (Haffajee 2000)
- 36. Coagregación bacteriana Actinomyces, un complejo amarillo que consta de miembros del género Streptococcus, un complejo verde compuesto por especies de Cap- nocytophaga, Actinobacillus actinomycete mcomitans serotipo a, Eikenella corrodens, Campylobacter conci- sus y un complejo púrpura consistente en Veillonella parvula y Actinomyces odontolyticus. Estos grupos de especies son colonizadores tempranos de la superficie del diente. P. gingivalis B. forsythus T. denticola C. gracilis C. rectus C. showae E. nodatum F. nucleatum nucleatum F. nucleatum polymorphum P. intermedia P. micros P. nigrescens S. constellatus Actinomyce s species S. mitis S. oralis S. sanguis Streptococcus sp. S. gordonii S. intermedius V. parvula A. odontolyticus E. corrodens C. gingivalis C. sputigena C. ochracea (Haffajee 2000)
- 37. Factores que afectan la adhesión del biofilm Físicas como la rugosidad de la superficie pueden incrementar el área de superficie y aumentar la colonización La rugosidad proporciona protección frente a las fuerzas de atrición y aumenta la dificultad de limpieza. composición química de una superficie repercute en la colonización bacteriana, por componentes dañinos. (Haffajee 2000)
- 39. Developing Mycobacterium smegmatis (Labeled view) American Society For Microbiology ©
- 40. Mature Mycobacterium smegmatis (Labeled view) American Society For Microbiology ©
- 41. Bibliografía Aduse-Opoku J, Slaney JM, Hashim A, Gallagher A, Gallagher RP, Rangarajan M, et al. Identification and characterization of the capsular polysacharide (K-antigen) locus of Prophyromonas gingivalis. Infect Immun 2006; 74: 449-60 Haffajee AD Socransky SS.Microbial etiological agents of destructive periodontal diseases. Periodontol 2000 1994:5: 78-111. Lindhe Jan. Periodontología Clínica e Implantología Odontológica. 3era Ed. Edit. Panamericana. (2000). Caps. 3 y 4 Socransky SS, Haffajee AD CuginiMA, Smith C. Microbial complexes in subgingival plaque. J C lin Periodontol 1998: 25: 134-144 Valle, J., Toledo-Arana, A., Berasain, C., Ghigo, J.M., Amorena, B., Penades, J.R., and Lasa, I. (2003) SarA and not σB is essential for biofilm development by Staphylococcus aureus. Mol Microbiol 48: 1075-1087