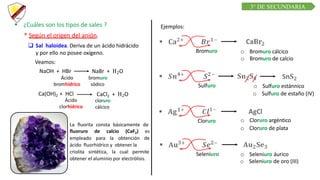
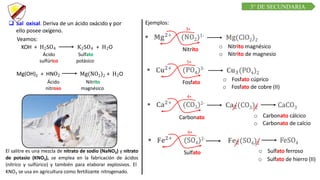
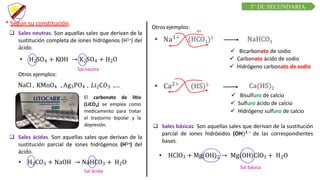
Este documento presenta información sobre la nomenclatura inorgánica III para estudiantes de 3er grado de secundaria. Los objetivos son relacionar la fórmula química y nomenclatura de cationes, aniones y sales según criterios de la IUPAC. Explica conceptos como iones, ácidos hidrácidos y oxácidos, y cómo se obtienen y nombran aniones, cationes y diferentes tipos de sales como sales haloideas y oxisales.





![C R E E M O S E N L A E X I G E N C I A
C U R S O D E Q U í M I C A
Los extintores de polvo químico seco se componen de
gases presurizados (CO2 + N2) y de una mezcla de varias
sales como son: bicarbonato sódico (NaHCO3),
bicarbonato potásico (KHCO3), dihidrógeno fosfato de
amonio [ (NH4)H2PO4] y cloruro potásico (KCl); estas
últimas sometidas a alta temperatura forman un material
viscoso, logrando así aislar el incendio del oxígeno.
La pila seca o pila de Leclanché, es un dispositivo que
produce energía eléctrica y permite el funcionamiento de:
la calculadora, reloj, control remoto, linterna, etc. Esta pila
requiere además de un cátodo (−) y un ánodo (+), la
presencia de un medio conductor eléctrico (electrolito)
constituido por una pasta de: cloruro de amonio (NH4Cl),
cloruro de zinc (ZnCl2), almidón y agua.
... Pero claro que hay más aplicaciones de las sales.
3° DE SECUNDARIA](https://image.slidesharecdn.com/cap18-qumica-3rosec-230221211718-079aba36/85/Cap18-quimica-3ro-Sec-pptx-6-320.jpg)