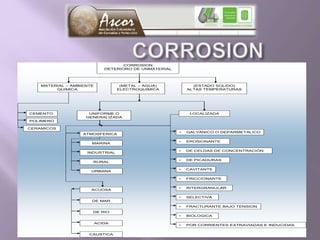
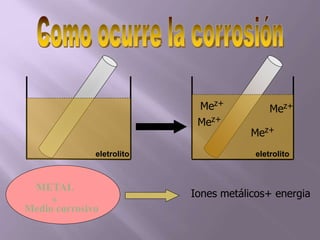
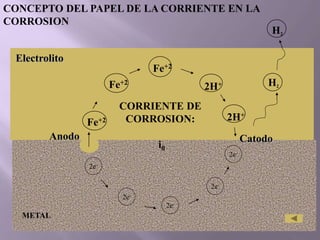
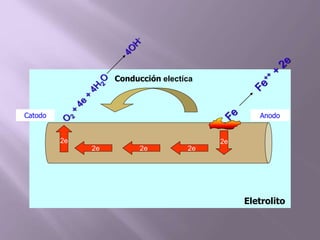
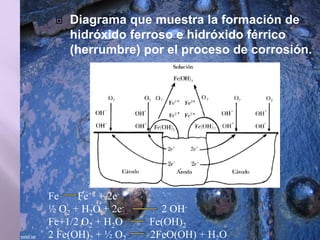
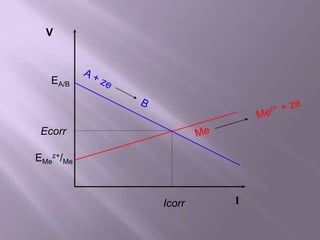
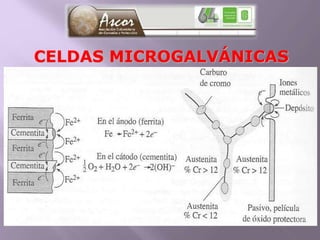
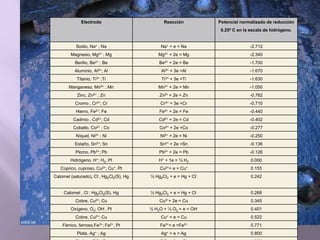
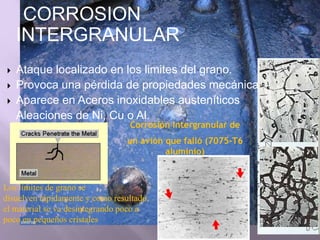
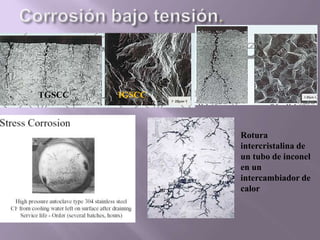
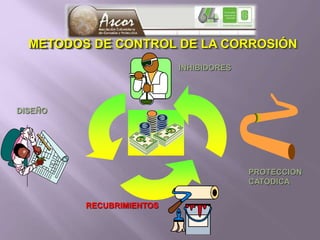
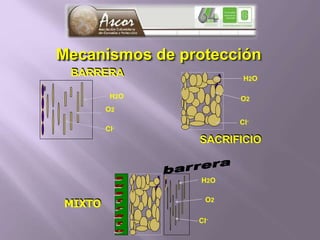
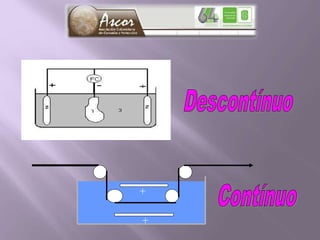
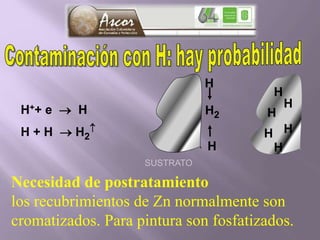
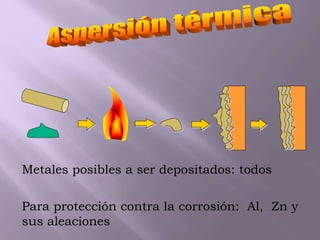
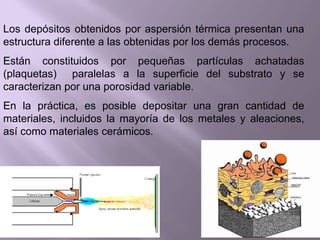
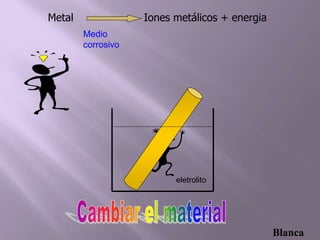
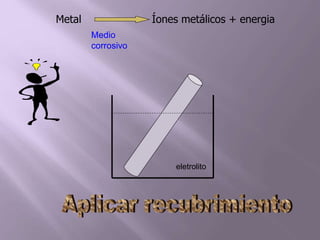
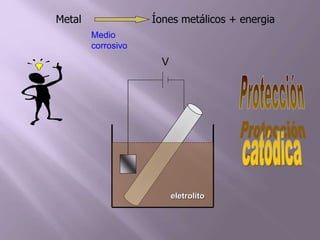
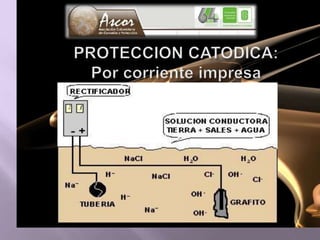
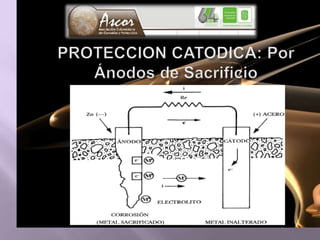
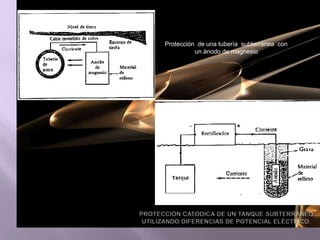
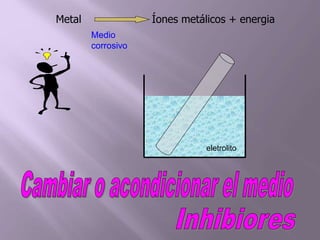
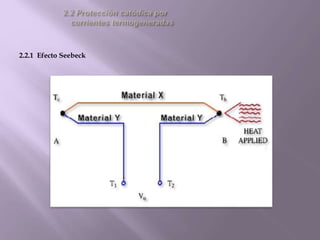
La corrosión es el deterioro de materiales sólidos, principalmente metales, debido a reacciones químicas o electroquímicas con su entorno. Los recubrimientos son cruciales para prevenirla, y pueden ser metálicos, orgánicos o inorgánicos, cada uno con diferentes métodos de aplicación y control de eficacia. Se abordan varios tipos de corrosión, incluyendo la uniformemente distribuida, localizada, intergranular y bajo tensión, así como métodos de protección como la protección catódica y el uso de inhibidores.