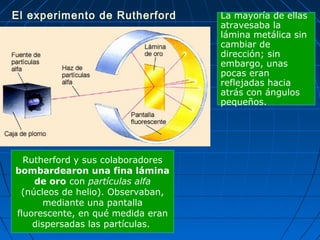
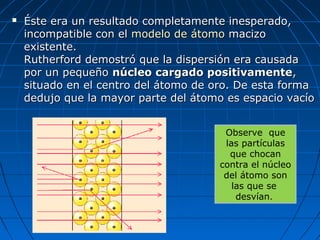
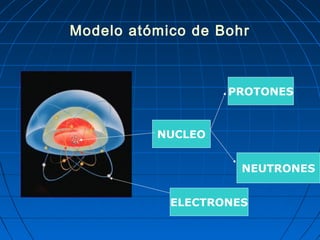
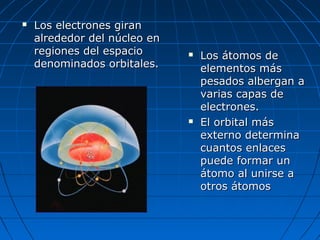
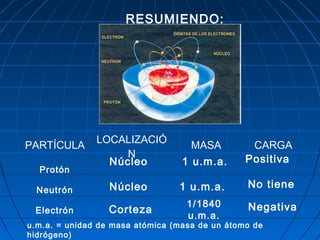
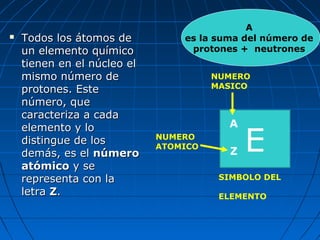
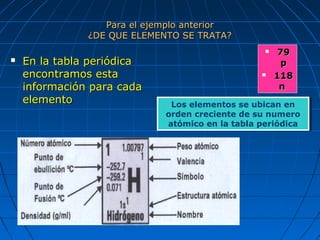
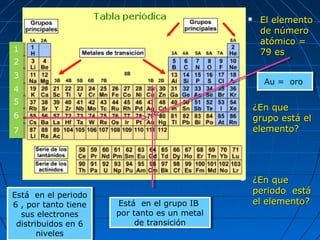
El documento resume la evolución del modelo atómico a través de los años. Demócrito propuso originalmente que la materia estaba compuesta de átomos indivisibles. Las ideas de Demócrito fueron retomadas por Dalton en el siglo XIX. Posteriormente, experimentos de Thomson, Rutherford y Bohr llevaron al desarrollo del modelo atómico moderno, en el que los átomos consisten en un núcleo central rodeado de electrones.