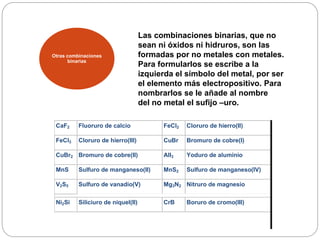
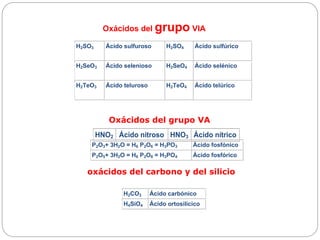
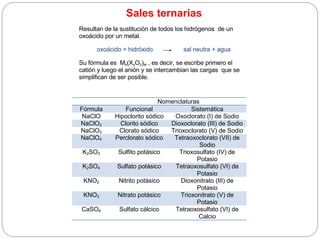
Este documento trata sobre la nomenclatura química inorgánica. Explica los diferentes tipos de compuestos inorgánicos como sustancias simples, óxidos, hidruros, sales y ácidos. También define los principales cationes, aniones y grupos funcionales como peróxidos e hidróxidos, y proporciona ejemplos de cada tipo de compuesto.