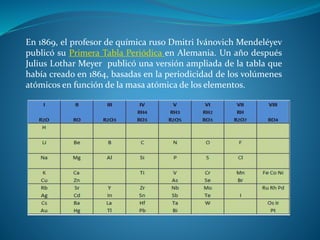
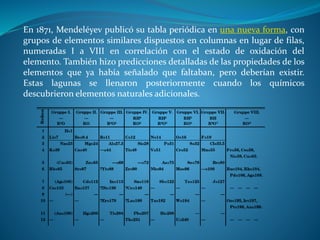
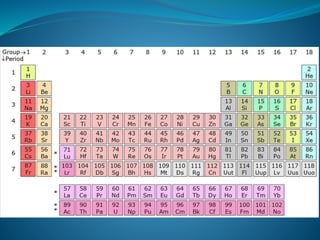
Este documento resume la importancia y el desarrollo de la tabla periódica de los elementos. Explica que la tabla ordena los elementos químicos por su número atómico y propiedades periódicas, y fue desarrollada por científicos como Mendeléyev en el siglo XIX. También destaca que la tabla periódica presenta la información sobre los elementos de una manera fácil de comprender y es una herramienta útil para la química y otras ciencias.