The chemistry of life - La quimica de la Vida
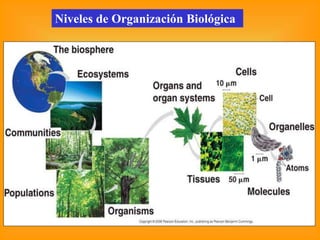
- 1. Niveles de Organización Biológica
- 3. LA BASE QUÍMICA DE LA VIDA
- 4. Los seres vivos son un conjunto de elementos, sustancias fundamentales que constan de una sola clase de átomos
- 5. La química celular se basa en los compuestos de carbono Célula Hidrógeno Carbono Nitrógeno Oxígeno Constituyen aproximadamente el 99% de su peso
- 6. La materia esta constituida por combinaciones de elementos 92 elementos Carbono Alotropía (del griego: allos, otro, y tropos, manera) en química es la propiedad que poseen determinados elementos químicos de presentarse bajo estructuras moleculares diferentes Diamante y grafito Fulerenos Oxígeno
- 7. La materia esta constituida por combinaciones de elementos Calcio Hierro
- 8. Abundancia de algunos elementos químicos en la corteza terrestre, comparada con su abundancia en los tejidos de un animal
- 9. El átomo Es la unidad más pequeña que conserva las propiedades del elemento. Ocupa espacio, tiene masa y no puede dividirse en otras partes.
- 10. Que es un elemento? Es una sustancia fundamental que consta de una sola clase de átomos. La carga eléctrica llevada por cada protón es exactamente igual y opuesta a la carga llevada por un solo electrón. Número atómico: El número de protones del núcleo de un átomo determina su identidad.
- 11. Tabla periódica de los elementos. Dimitry Mendeleev
- 12. Isótopos: Cada isótopo tiene diferente número de neutrones pero el mismo número de protones y electrones. Son átomos del mismo elemento con masa distinta Carbono 14 es inestable y radiactivo. Es usado en arqueología para determinar el tiempo y origen de los materiales orgánicos. Decaimiento radiactivo: emite espontáneamente energía en forma de partículas subatómicas y rayos cuando su núcleo se desintegra. Se convierte en un producto mas estable
- 13. Que sucede cuando un átomo se enlaza a otro? POR QUÉ LOS ELECTRONES SON IMPORTANTES? Los átomos adquieren, comparten y liberan electrones. El número y el orden de sus electrones determinará si se une o no a otros.
- 14. DE LOS ÁTOMOS A LAS MOLÉCULAS Las partículas constituidas por dos o más átomos se conocen como moléculas y las fuerzas que las mantienen unidas se conocen como enlaces. Hay dos tipos principales de enlaces: iónico y covalente
- 15. Enlaces Iónicos: Ganancia o pérdida de electrones Ión: un átomo que ha ganado o perdido electrones adquiere una carga Na+ y Cl–.
- 16. K+ : en su presencia puede ocurrir la mayoría de los procesos biológicos esenciales. Ca2+, K+ y Na+: están implicados en la producción y propagación del impulso nervioso. Importancia de los iónes
- 17. Ca2+ : es necesario para la contracción de los músculos y para el mantenimiento de un latido cardíaco normal. Mg2+: forma parte de la molécula de clorofila, la cual atrapa la energía radiante del Sol en algunas algas y en las plantas verdes Importancia de los iónes
- 18. Enlace covalente
- 19. Importancia de los iones ¿Por qué, cuando la vida se organizó y evolucionó, fueron estos elementos tan importantes?
- 20. COMPOSICIÓN QUÍMICA DE LA CÉLULA La sustancia mas abundante de la célula es el agua
- 21. Agua y soluciones La mayoría de las reacciones intracelulares ocurren en un medio acuoso. La vida en este planeta inició en el mar y las condiciones que reinaban en aquel ambiente primitivo imprimieron un sello permanente en la química de la materia viva. Todos los organismos han sido diseñados en base a las propiedades características del agua
- 22. Propiedades del Agua Carácter polar Capacidad de formar puentes de hidrógeno. Alta tensión superficial
- 23. La estructura del agua Enlace covalente Molécula polar Puentes de hidrógeno
- 24. Los puentes de hidrógeno determinan las propiedades del agua Los puentes de hidrógeno son responsables de la cohesión o atracción mutua de sus moléculas- alta tensión superficial
- 25. La pérdida de agua por evaporación ayuda a los mamíferos a enfriarse al sudar Los puentes de hidrógeno son responsables de su resistencia a los cambios de temperatura: alto calor específico o capacidad calorífica, alto calor de vaporización y alto calor de fusión EFECTOS ESTABILIZADORES DE LA TEMPERATURA DELAGUA
- 26. Propiedades Físico - Químicas del agua Acción disolvente El agua es el medio en que transcurren las mayoría de las reacciones del metabolismo, y el aporte de nutrientes y la eliminación de desechos se realizan a través de sistemas de transporte acuosos.
- 27. La polaridad de la molécula del agua La polaridad es responsable de su adhesión a otras sustancias polares: movimiento capilar
- 28. Elevada fuerza de adhesión. Capilaridad
- 29. Hidrofílicas: azucares, ADN, ARN y la mayoría de las proteínas
- 30. ÁCIDOS BASES El agua tiene una ligera tendencia a ionizarse Casi todas las reacciones químicas de los sistemas vivos tienen lugar en un estrecho intervalo de pH alrededor de la neutralidad. Los organismos mantienen este estrecho intervalo de pH por medio de buffers, que son combinaciones de formas de ácidos débiles o bases débiles; dadores y aceptores de H+. H+, pH < 7 OH-, pH > 7
- 31. Las funciones del agua se relacionan íntimamente con las propiedades anteriormente descritas. Se podrían resumir en los siguientes puntos Soporte o medio donde ocurren las reacciones metabólicas. Amortiguador térmico. Transporte de sustancias. Lubricante, amortiguadora del roce entre órganos. Favorece la circulación y turgencia. Da flexibilidad y elasticidad a los tejidos Puede intervenir como reactivo en reacciones del metabolismo, aportando hidrogeniones o hidroxilos al medio. Funciones del agua ( Resumen)
- 32. Moléculas orgánicas Carbono, Hidrógeno y Oxígeno. Además, las proteínas contienen Nitrógeno y Azufre, y los nucleótidos, así como algunos lípidos, contienen Nitrógeno y Fósforo. Todas estas moléculas contienen
- 33. Carbohidratos
- 34. El gliceraldehído, la ribosa y la glucosa contienen, además de los grupos hidroxilo, un grupo aldehído, que se indica en violeta; se llaman azúcares de aldosa (aldosas). La dihidroxiacetona, la ribulosa y la fructosa contienen un grupo cetona, indicado en pardo, y se llaman azúcares de cetosa (cetosas).
- 35. Los azúcares simples Carbohidratos (CH2O)n. C= “carbo” y H2O= “hydrate
- 36. α ó β, depende de la configuración del carbono 1.
- 37. Monosacáridos: no pueden ser hidrolizados Hidrolizar: separación de una molécula en dos o mas moléculas menores por reaccionar con el agua Glucosa. Fuente de energía. Fructosa. Galactosa
- 40. Maltosa.- Es el azúcar de malta. Grano germinado de cebada que se utiliza en la elaboración de la cerveza. Se obtiene por hidrólisis de almidón y glucógeno. Posee dos moléculas de glucosa unidas por enlace tipo α (1-4).
- 41. Lactosa.- Es el azúcar de la leche de los mamíferos. Así, por ejemplo, la leche de vaca contiene del 4 al 5% de lactosa. Se encuentra formada por la unión β (1-4) de la -D-galactopiranosa (galactosa) y la -D- glucopiranosa (glucosa).
- 43. MALTOSA Glucosa-α(1→4)-Glucosa ISOMALTOSA Glucosa-α(1→6)-Glucosa CELOBIOSA Glucosa-β(1→4)-Glucosa LACTOSA Galactosa-β(1→4)-Glucosa TREHALOSA Glucosa-α(1→1)-Glucosa SACAROSA Fructosa-β(2→1)-Glucosa
- 44. Polisacáridos Los carbohidratos sirven como fuente de energía, combustible e intermediarios metabólicos. Funciones
- 45. Almidón: Reserva energética en los amiloplastos Polisacaridos: formas de almacenar los carbohidratos en animales y plantas
- 46. Glucógeno
- 47. Celulosa. Es el principal componente estructura de la pared celular de plantas.
- 48. Celulosa
- 49. Quitina
- 50. Los carbohidratos se unen a proteínas y lípidos: Señal de reconocimiento en superficie
- 52. Azúcares como la ribosa y deoxiribosa forman parte de la estructura del RNA y DNA La flexibilidad conformacional de los anillos de estos azúcares es importante en el almacenamiento y expresión de la información genética
- 53. Aminoácidos y Proteínas Están formadas, al menos, por cuatro bioelementos: C, H, O y N.
- 54. Aminoácidos Moléculas orgánicas con un grupo carboxilo y un grupo amino. Al carbono se unen además un átomo de hidrógeno y una cadena R, que distingue a los diferentes aminoácidos.
- 56. Enlace peptídico Este enlace resulta de la formación de un grupo amida entre el grupo alfa-carboxilo de un Aa y el grupo alfa-amino de otro.
- 57. Aminoácidos esenciales Fenilalanina Aprendizaje, memoria, control de apetito, deseo sexual, estados de ánimo, recuperación y desarrollo de tejidos, sistema inmunológico y control del dolor). Metionina Rendimiento muscular, remover del hígado residuos de procesos metabólicos, ayudar a reducir las grasas y a evitar el depósito de grasas en arterias y en el hígado. Histidina Crecimiento y reparación de tejidos, en la formación de glóbulos blancos y rojos. Propiedades antiinflamatorias Triptófano Ayuda a controlar el normal ciclo de sueño, tiene propiedades antidepresivas, incrementa los niveles de somatotropina permitiendo ganar masa muscular magra e incremento de la resistencia.
- 58. Treonina Componente importante del colágeno, esmalte dental y tejidos. Propiedades antidepresivas. Es un agente lipotrópico, evita la acumulación de grasas en el hígado. Leucina Formación y reparación del tejido muscular. Isoleucina Las mismas propiedades que la Valina, pero también regula el azúcar en la sangre e interviene en la formación de hemoglobina. Lisina Es necesaria para un buen crecimiento, desarrollo de los huesos, absorción del calcio, formación de colágeno, encimas, anticuerpos, ayuda en la obtención de energía de las grasas y en la síntesis de las proteínas. Valina Forma parte integral del tejido muscular, puede ser usado para conseguir energía por los músculos en ejercitación, posibilita un balance de nitrógeno positivo e interviene en el metabolismo muscular y en la reparación de tejidos).
- 59. Aminoácidos no esenciales Alanina (Interviene en numerosos procesos bioquímicos del organismo que ocurren durante el ejercicio, ayudando a mantener el nivel de glucosa). Acido aspártico (Ayuda a reducir el nivel de amoníaco en sangre después del ejercicio). Glicina (Es utilizada por el hígado para eliminar fenoles (tóxicos) y para formar sales biliares. Es necesario para el correcto funcionamiento de neurotransmisores y del sistema nervioso central. Incrementa el nivel de creatina en los músculos y también de las somatotrofinas; de esta manera es posible beneficiarse con un incremento en la fuerza y masa muscular). Serina (Es fundamental en la formación de algunos neurotransmisores, en la metabolización de las grasas y para mantener un buen nivel del sistema inmunológico). Asparragina (Interviene específicamente en los procesos metabólicos del Sistema Nervioso Central).
- 60. Acido glutámico (Tiene gran importancia en el funcionamiento del Sistema Nervioso Central y actúa como estimulante del sistema inmunológico). Arginina (Estimula la liberación de hormonas del crecimiento. Reduce la grasa corporal, mejor recuperación y cicatrización de heridas y un mayor incremento de la masa muscular). Cistina (Es importante en la formación de cabello y piel y también es un agente desintoxicante del amoníaco). Tirosina (Interviene en distintos procesos de regulación del apetito, sueño, reducción del stress. También es un buen antidepresivo y reductor de grasa corporal). Cisteina (Está implicada en la desintoxicación, principalmente como antagonista de los radicales libres. También contribuye a mantener la salud de los cabellos por su elevado contenido de azufre). Glutamina (Se detalla más abajo). Prolina (Es de fundamental importancia para un saludable estado de los tejidos de colágeno, piel, tendones y cartílagos).
- 61. PROPIEDADES DE LAS PROTEÍNAS Solubilidad Esta propiedad es la que hace posible la hidratación de los tejidos de los seres vivos. Capacidad amortiguadora Las proteínas tienen un comportamiento anfótero y esto las hace capaces de neutralizar las variaciones de pH del medio, ya que pueden comportarse como un ácido o una base y por tanto liberar o retirar protones (H+) del medio donde se encuentran.
- 62. PROPIEDADES DE LAS PROTEÍNAS Desnaturalización y renaturalización En estos casos las proteínas se transforman en filamentos lineales y delgados que se entrelazan hasta formar compuestos fibrosos e insolubles en agua. Los agentes que pueden desnaturalizar a una proteína pueden ser: calor excesivo; sustancias que modifican el pH; alteraciones en la concentración; alta salinidad. Pierden su actividad biológic
- 64. Función estructural ·Algunas proteínas constituyen estructuras celulares. ·Ciertas glucoproteínas forman parte de las membranas celulares y actúan como receptores o facilitan el transporte de sustancias. ·Las histonas, forman parte de los cromosomas que regulan la expresión de los genes. ·Otras proteínas confieren elasticidad y resistencia a órganos y tejidos: ·El colágeno del tejido conjuntivo fibroso. ·La elastina del tejido conjuntivo elástico. ·La queratina de la epidermis. ·Las arañas y los gusanos de seda segregan fibroina para fabricar las telas de araña y los capullos de seda, respectivamente.
- 65. ESTRUCTURAS DE LAS PROTEÍNAS Dos o más polipéptidos pueden actuar recíprocamente para formar una estructura cuaternaria.
- 66. Los puentes de hidrógeno entre los grupos C=O y NH tienden a plegar la cadena en una estructura secundaria repetida la hélice alfa. la hoja plegada beta
- 67. Las interacciones entre los grupos R de los aminoácidos pueden dar como resultado un plegamiento ulterior en una estructura terciaria, que a menudo es de forma globular e intrincada
- 68. El papel central del carbono