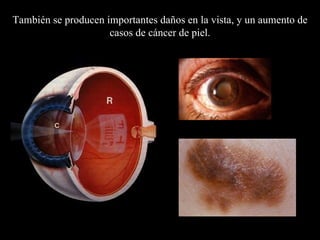
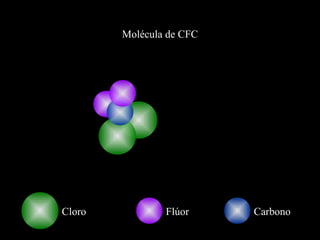
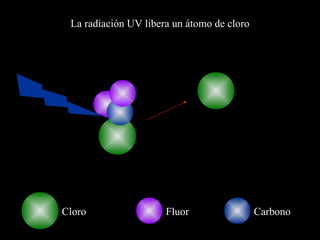
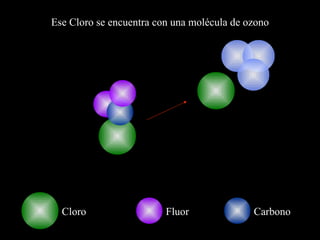
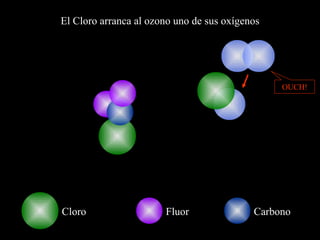
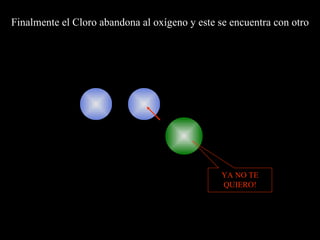
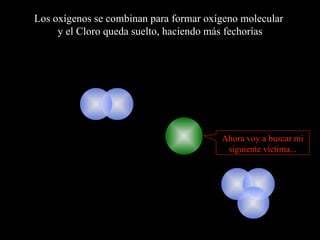
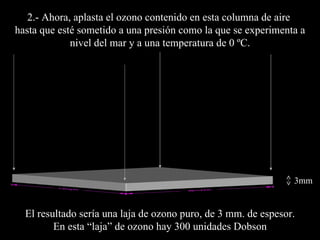
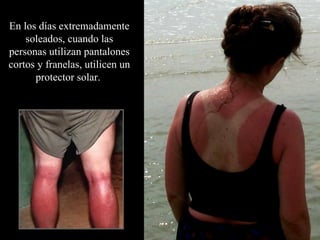
El documento describe la capa de ozono, incluyendo su origen, composición química, ubicación en la atmósfera, y función de proteger la vida en la Tierra de la radiación ultravioleta del Sol. También explica cómo los clorofluorocarbonos (CFC) emitidos por actividades humanas degradan la capa de ozono, y los esfuerzos internacionales para regular los CFC y permitir la recuperación de la capa de ozono.













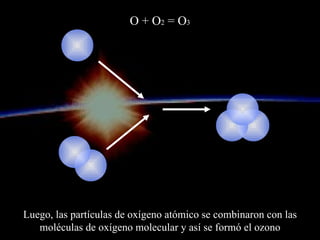










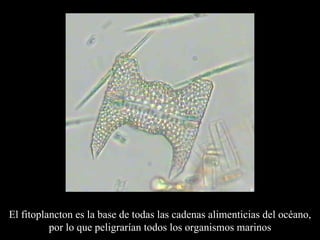
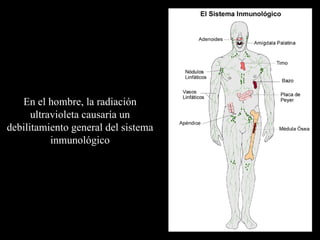





















































![GRACIAS [email_address]](https://image.slidesharecdn.com/tierracapadeozonolonniepacheco2008-1227465262781375-9/85/Tierra-Capa-De-Ozono-Lonnie-Pacheco2008-95-320.jpg)

