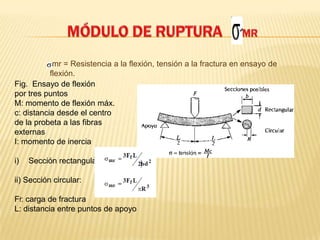
Los cerámicos están constituidos por átomos de elementos metálicos y no metálicos unidos químicamente. Presentan estructuras cristalinas compuestas de cationes y aniones, determinadas por la carga eléctrica de los iones y sus tamaños relativos. Los silicatos, como la sílice, forman tetraedros de SiO4 unidos por cationes. El carbono existe en formas como grafito y diamante, con átomos unidos por enlaces covalentes. Los cerámicos se fracturan de modo frágil y su ten