Influencia de los fotoperiodos en variables morfológicas histológicas y citológicas en la germinación de la lafoencia acuminata
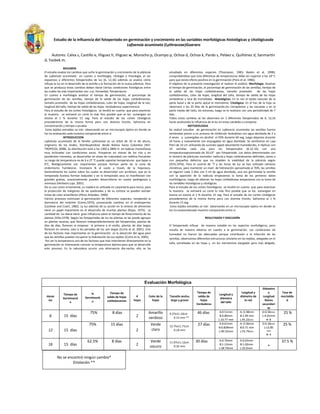
- 1. -565150-363855Estudio de la influencia del fotoperiodo en germinación y crecimiento en las variables morfológicas histológicas y citológicas de Lafoensia acuminata (Lythraceae) Guararo<br />Autores: Calva s, Castillo e, Iñiguez h, Iñiguez w, Morocho p, Ocampo p, Ochoa d, Ochoa k, Pardo s, Peláez v, Quiñónez d, Sanmartín d, Yasbek m.<br />RESUMEN<br />El estudio evalúa los cambios que sufre la germinación y crecimiento de la plántula de Lafoensia acuminata en cuanto a morfología, citología e histología; al ser expuestas a diferentes fotoperiodos de luz (6, 12,16) además se analiza cómo influye la luz en el desarrollo de la semilla y la formación de la nueva plántula. Para que se produzca estos cambios deben darse ciertas condiciones fisiológicas entre las cuales las más importantes son: Luz, Humedad, Temperatura.<br />En cuanto a morfología analizar el tiempo de germinación, el porcentaje de germinación de las semillas, tiempo de la salida de las hojas cotiledónareas, tamaño promedio de las hojas cotiledónareas, color de hojas, longitud de la raíz, longitud del tallo, tiempo de salida de las hojas verdaderas y supervivencia<br />Para el estudio de los cortes histológicos se tendrá en cuenta que para examinar la muestra se extraerá un corte lo más fino posible que se los sumergían en eosina al 1 % durante 15 seg. Para el estudio de los cortes citológicos procederemos de la misma forma pero con distinta tinción, Safranina en concentración y tiempo a prueba. <br /> Estos tejidos extraídos se irán observando en un microscopio óptico en donde se los ira evaluando cada muestra comparando entre sí.<br />INTRODUCCION<br />Lafoensia acuminata de la familia Lythraceae es un árbol de 10 m de altura, originario de los Andes, distribuyéndose desde Bolivia hasta Colombia (W3-TROPICOS, 2008). Su distribución está a los 1300 a 2800 m en laderas montañosas muy inclinadas con condiciones secas. Prosperan en riveras de los ríos y en pendientes húmedos, se desarrollan en áreas de nubosidad con neblina frecuente su rango de temperatura va de 4 a 27 °C puede soportar temperaturas que bajan a 0°C. Biológicamente son importantes porque forman parte de la zona de endemismo Tumbesino. Incorpora N al suelo a través de la hojarasca. Generalmente los suelos sobre los cuales se desarrollan son arcillosos, que en la temporada lluviosa forman lodazales y en la temporada seca se manifiestan con grandes grietas, ocasionalmente pueden desarrollarse en suelos pedregosos y arenosos (Herbario Loja. 2001)<br />De su uso como ornamental, su madera es utilizada en carpintería para torno, para la protección de márgenes de las quebradas y de su corteza se pueden extraer tintes de color amarillento (Pérez-Arbeláez, 1990).<br />Ciertos procesos estimulan la germinación de diferentes especies, rompiendo la dormancia del embrión (Come, 1970), provocando cambios en el endospermo (Locklear and Coort, 1982). La luz además de su acción en la síntesis de alimentos tiene un papel importante en el desarrollo de muchas plantas (Rojas, 1973). La cantidad de luz diaria tiene gran influencia sobre el tiempo de florecimiento de las plantas (Ville, 1978). Según los fotoperiodos de luz las plantas se las puede agrupar en plantas neutras, que florecen independientemente del fotoperiodo, plantas de días de días, florecen al empezar la primera o el otoño, plantas de días largos florecen en verano, solo si los periodos de luz son largos (Curtis et al, 2001). Uno de los factores más importantes en la germinación es la absorción del agua para que las semillas puedan recuperar la hidratación de sus tejidos (Curtis et la, 2005).<br /> Por ser la temperatura uno de los factores que más intervienen directamente en la germinación es interesante conocer la temperatura óptima para que se desarrolle este proceso. En la naturaleza ocurre una alternancia día-noche, ello se ha estudiado en diferentes especies (Thompson, 1983; Baskin et al, 1998), comprobándose que esta diferencia de temperaturas debe ser superior a los 10° C para que exista efecto positivo en la germinación (Pons et al, 1986).<br />El objetivo de la presente investigación el realizar el análisis: Morfología: Analizar el tiempo de germinación, el porcentaje de germinación de las semillas, tiempo de la salida de las hojas cotiledónareas, tamaño promedio de las hojas cotiledónareas, color de hojas, longitud del tallo, tiempo de salida de las hojas verdaderas y tasa de mortalidad. Histológicos: En la raíz el tejido vascular de la parte basal y de la parte apical el meristemo. Citológico: En el haz de la hoja se observara a los 25 días de la germinación, los cloroplastos y las vacuolas y en la parte media del tallo, los estomas, luego se lo realizara con una periodicidad de 7 días.<br />Todos estos cambios se los observara en 3 diferentes fotoperiodos de 6, 12,16 horas analizando la influencia de la luz en estas variables a comparar.<br />METODOLOGIA<br />Se realizó estudios de germinación en Lafoencia acuminata las semillas fueron sembradas previo a un proceso de inhibición lavándolas con agua destilada de 2 a 4 veces y sumergidas en alcohol al 93% durante 60 seg, luego dejamos durante 24 horas y nuevamente son enjuagadas en agua destilada. Se sembraron en caja Petri de 10 cm utilizando de sustrato papel absorbente humedecido, 4 réplicas con 10 semillas cada una para los fotoperiodos (6-12-16) con una temperatura aproximada de 20-23° por fotoperiodo .Los datos determinados son el número de plántulas normales: radícula y hojas cotiledonarias definidos, sanos o con pequeños defectos que no impiden la viabilidad de la plántula según (ISTA.1976). Para el control de °T y las horas de luz se han utilizado cámaras climáticas, para mantener un nivel de hidratación aproximado al 70%, las semillas se regaron cada 3 días con 5 ml de agua destilada, una vez germinada la semilla con la aparición de la radícula empezamos la toma de los primeros datos morfológicos, luego de obtener las hojas cotiledóneas empezamos con la toma de las variables histológicas y citológicas.<br />Para el estudio de los cortes histológicos se tendrá en cuenta que para examinar la muestra se extraerá un corte lo más fino posible que se los sumergían en eosina en eosina al 1 % durante 15 seg. Para el estudio de los cortes citológicos procederemos de la misma forma pero con distinta tinción, Safranina al 1 % durante 15 seg. <br /> Estos tejidos extraídos se irán observando en un microscopio óptico en donde se los ira evaluando cada muestra comparando entre sí.<br />RESULTADOS Y DISCUSIÓN<br />El fotoperiodo influye de manera notable en los aspectos morfológicos, pero resulta de manera adversa en cuanto a la germinación. Las condiciones de humedad no fueron las adecuadas porque contribuían a la infección de las semillas, observamos diferentes estructuras celulares en los tejidos, alargadas en el tallo, estrelladas en las hojas y en los meristemos alargadas pero más delgada.<br />Evaluación MorfológicaHoras luzTiempo de Germinación%GerminaciónTiempo de salida de hojas cotiledonareas# hojasColor de la hojasTamaño ancho, largo y grosorTiempo de salida de hojas VerdaderasLongitud y diámetro del talloLongitud y diámetro de la raízDiámetro y Longitud Raíces secundariasTasa de mortalidad615 días 75% 8 días2Amarillo verdoso9.27x11.10cm 0.13 mm ** 46 días A:0.51mmB:0.89mmL:10.77 mmA: 0.38mmB:1.09 mmL:45.22mmD:0.30mmL:4.01mm#: 8 25 %1215 días75%15 días2Verde claro12.75x11.71cm 0.18 mm27 díasA:0.61mmB:0.838mmL:40.32mmA: 0.36mmB:0.71 mmL:55.79mmD:0.18mmL:12.85mm#: 425 %1615 días62.5%8 días2Verde oscuro11.97x11.12cm 0.32 mm 30 díasA:0.76mmB:1.12mmL:38.79mmA:0.65mmB:1.02mmL:35.0mm*37.5 %<br />No se encontró ningún cambio* Etiolación ** <br /> Observaciones CitológicasHistológicasFotoperiodoCloroplastos Vacuola EstomasMeristemo basal de la raízMeristemo apical de la raíz25d32d 39d25d32d39d25d32d39d25d32d39d25d32d39d645*66***T: 23H: 7*H:256T:30*******12**202***T: 89*T:82*65******16*137***1T: 19*T: 50*******No se encontró organela o tejido *<br />Conclusiones<br />En Lafoencia acuminata. <br />El fotoperiodo 6 provoco un fenómeno de etiolación en un 90 % a las plántulas.<br />En el fotoperiodo 2 fue el más apropiado en la germinación y desarrollo óptimo de la plántula.<br />En el fotoperiodo 3 causo mayor tasa de mortandad.<br />En el color de las plántulas de los diferentes fotoperiodos se notó una gran diferencia.<br />Bibliografía<br />Baskin, c. Baskin, j. 1998. Seed. Ecology, biogeography and evolution of dormancy and germination, academic press. Pp.666. combinations of gibberellin, scarification, light and dark. Scientia horniculturae 59: 243-252 <br />Cermeño P.; Corell, M, García M C,; Jorge Olave, J,; Guzman, M. and Sánchez, A., 2006. Effect of temperature, lighy and GA3 aplication on germination of Salvia lavandulifolia Vahl. Acta Horticulturae. En prensa<br />Cermeño P.; Corell, M, García C., Sanchez A and Guzman M. 2007. Influencia del Fotoperiodo en la germinación de Santolina rosmarinifolia y Santolina chamaecyparissus. Sección de Horticultura. C.I.F.A “Las Torres-Tomejil” IFAPA Consejería de Innovación y Empresas. Ctra. Sevilla – Alcalá del Río Km. 12,2.Dep, Producción Vegetal, Universidad de Almería. Pág. 477- 480<br />Cermeño P,. Del Olmo, L..A., Corell, M. And Belda, J., 2002. Pregermination and Germionation in Asparagus. Acta Horticulturae. International Society for Horticultural Science. Belgium. Vol.589:341-345<br />Cermeño P,. Del Olmo, L..A.,Calero, I,. Calado, S., Belda, J., 2002 Influencia de la temperature de germinación en Bellis perennis L. I Jornadas Científicas Ibéricas de Plantas Ornamentales , SECH Y APH: Consejería Agricultura y Pesca de Andalucía. Sevilla.165-172.<br />Cermeño P,. Del Olmo, L..A.,Calero, I,. Calado, S., Belda, J., 2002 Influencia de la temperature de germinación en Bellis perennis L. I Jornadas Científicas Ibéricas de Plantas Ornamentales , SECH Y APH: Consejería Agricultura y Pesca de Andalucía. Sevilla. 173-180.<br />Cermeño P,. Del Olmo, L..A., Corell, M. And Belda, J. Temperature y Germinación Asparagus officinalis L. Seminario de Técnicos y especialistas en Horticultura. Madrid 143-148 (1.999)<br />Côme D., 1970. Les obstacles á la germination. Masson, Paris. International Seed Testing Assosition (ISSTA), 1976. Reglas Internacionales para Ensayos de Semillas. Ministerio de Agricultura España.<br />Curtis,h .Barnes, n. Schenek, a. Massarini,a.2001.Biología. sexta edición. panamericana. España. Pp. 1023<br />Leopold, a.1964.crecimiento vegetal y desarrollo. McGraw-Colina. Nueva york. Pp. 183<br />Locklear J. h. and Coorts G.D., 1982. The container production of herbaceous perennials. BPI NEWS 12. 3-5<br />Pons T. and Schoroder H., 1986. Significance of temperature fluctuation and oxygen concentration for germination of the rice field weeds Fimbristylis littoralis and Scirpus Juncoides. Oecologia 68: 315-319.<br />Raven, p. Vuelque, y Eichhorn, s.2005. Biología de las plantas.7 edición. Nueva york. Pp. 9<br />Rojas, G.1973. Fisiología vegetal aplicada. 4 edición. Pp. 213<br />Solomon, E. Martin, d. 1996. Biología. Interamericana. México. Pp.692-697<br />Testing Association (ISTA). 1976. Reglas internacionales para ensayos de semillas. Ministerio de agricultura .España. Pp. 184<br />Thompson K and Grime J.P., 1983. A comparative study of germination responses to diurnally – fluctuating temperatures. J. Appl. Ecol. 20: 141 – 156<br />