Modelo atómico de bohr animado.ok
•Descargar como PPT, PDF•
4 recomendaciones•34,339 vistas
Power point animado sobre el modelo atómico de Bohr y su comparación con los otros modelos propuestos, incluido el cuántico.
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Similar a Modelo atómico de bohr animado.ok
Similar a Modelo atómico de bohr animado.ok (20)
Trabajo de fisica actividad modificacion 2 finalizados

Trabajo de fisica actividad modificacion 2 finalizados
Más de Hogar
Más de Hogar (20)
Replicación del DNA. Guía basada en la metodología POGIL.pdf

Replicación del DNA. Guía basada en la metodología POGIL.pdf
Dogma central de la biología molecular. Guía basada en la metodología POGIL.pdf

Dogma central de la biología molecular. Guía basada en la metodología POGIL.pdf
¿cómo interactúan los seres vivos? Guía basada en la metodología POGIL..pdf

¿cómo interactúan los seres vivos? Guía basada en la metodología POGIL..pdf
Sistema circulatorio. Guía basada en la metodología POGIL.pdf

Sistema circulatorio. Guía basada en la metodología POGIL.pdf
Inmunidad en procariotas. Guía basada en la metodología POGIL.pdf

Inmunidad en procariotas. Guía basada en la metodología POGIL.pdf
Morfología cromosómica eucariota.Guía basada en la metodología POGIL.pdf

Morfología cromosómica eucariota.Guía basada en la metodología POGIL.pdf
Crispr cas9, edición del genoma. Guía basada en la metodología POGIL.pdf

Crispr cas9, edición del genoma. Guía basada en la metodología POGIL.pdf
Ciclo sars cov2-2021. Guía basada en la metodología POGIL.

Ciclo sars cov2-2021. Guía basada en la metodología POGIL.
Fotosíntesis, Guía basada en la metodología POGIL, para primeros medios

Fotosíntesis, Guía basada en la metodología POGIL, para primeros medios
Movimiento de los continentes, guía basada en la metodología POGIL.

Movimiento de los continentes, guía basada en la metodología POGIL.
Carrera armamentista entre los animales. Guía basada en la metodología POGIL

Carrera armamentista entre los animales. Guía basada en la metodología POGIL
Objetos de nuestro sistema solar. Guía basada en la metodología POGIL.

Objetos de nuestro sistema solar. Guía basada en la metodología POGIL.
¿Cómo funciona el Dna? Guía de biología octavo de enseñanza básica, 

¿Cómo funciona el Dna? Guía de biología octavo de enseñanza básica,
Chi-cuadrado, guía para biólogos, basada en la Metodología POGIL

Chi-cuadrado, guía para biólogos, basada en la Metodología POGIL
Ciclo de vida de las estrellas, guía basada en la metodología POGIL

Ciclo de vida de las estrellas, guía basada en la metodología POGIL
Análisis de secuencias de aminoácidos para determinar relaciones evolutivas

Análisis de secuencias de aminoácidos para determinar relaciones evolutivas
Modelo atómico de bohr animado.ok
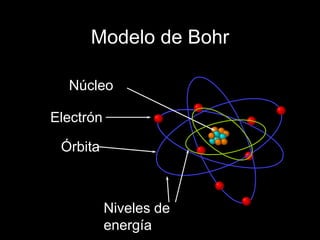
- 1. Modelo de Bohr Núcleo Electrón Órbita Niveles de energía
- 2. Modelo atómico de Bohr n=3 e- n=2 ee- n=1 ee- Aumento de la energía (Órbitas) e- e- e- e- e- eSe emite un fotón Con energía E = hf El modelo atómico de Bohr, como muchas ideas en la historia de la ciencia fue aceptado en un principio pero más tarde refutado por la experimentación. http://en.wikipedia.org/wiki/Category:Chemistry
- 3. Un modelo insatisfactorio para el átomo El físico danés Niels Bohr ( Premio Nobel de Física 1922), postula que los electrones giran a grandes velocidades alrededor del núcleo atómico. Los electrones se disponen en diversas órbitas circulares, las cuales determinan diferentes niveles de energía. El electrón puede acceder a un nivel de energía superior, para lo cual necesita "absorber" energía. Para volver a su nivel de energía original es necesario que el electrón emita la energía absorbida ( por ejemplo en forma de radiación). Este modelo, si bien se ha perfeccionado con el tiempo, ha servido de base a la moderna física nuclear.). Hill, Petrucci, General Chemistry An Integrated Approach 2nd Edition, page 294
- 4. Modelo cuántico Niels Bohr & Albert Einstein La teoría atómica moderna describe la estructura electrónica del átomo como la probabilidad de encontrar a los Electrones en ciertas regiones del espacio(orbitales).
- 5. Visión Moderna • El átomo es en su mayor parte espacio vacío • Tiene dos regiones: – Núcleo • Protones y neutrones – Nube electrónica • Región donde se puede encontrar los electrones
- 6. Mecánica cuántica • Orbital (“Nube electrónica”) – Región en el espacio donde hay un 90% de probabilidad de encontrar un electrón Probabilidad del electrón vs. Distancia 40 Probabilidad del Electrón (%) 90% de probabilidad de encontrar un electrón 30 20 10 0 0 50 100 150 Distancia del núcelo (pm) Orbital Courtesy Christy Johannesson www.nisd.net/communicationsarts/pages/chem 200 250
