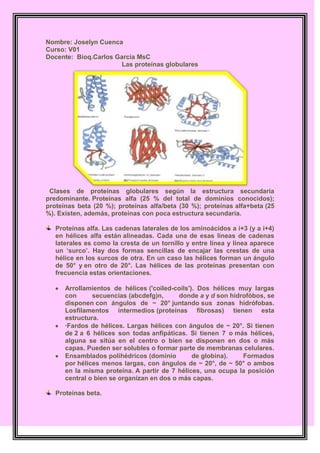
Proteinas globulares
- 1. Nombre: Joselyn Cuenca Curso: V01 Docente: Bioq.Carlos García MsC Las proteínas globulares Clases de proteínas globulares según la estructura secundaria predominante. Proteínas alfa (25 % del total de dominios conocidos); proteínas beta (20 %); proteínas alfa/beta (30 %); proteínas alfa+beta (25 %). Existen, además, proteínas con poca estructura secundaria. Proteínas alfa. Las cadenas laterales de los aminoácidos a i+3 (y a i+4) en hélices alfa están alineadas. Cada una de esas líneas de cadenas laterales es como la cresta de un tornillo y entre línea y línea aparece un ‘surco’. Hay dos formas sencillas de encajar las crestas de una hélice en los surcos de otra. En un caso las hélices forman un ángulo de 50° y en otro de 20°. Las hélices de las proteínas presentan con frecuencia estas orientaciones. Arrollamientos de hélices ('coiled-coils'). Dos hélices muy largas con secuencias (abcdefg)n, donde a y d son hidrofóbos, se disponen con ángulos de ~ 20° juntando sus zonas hidrófobas. Losfilamentos intermedios (proteínas fibrosas) tienen esta estructura. ·Fardos de hélices. Largas hélices con ángulos de ~ 20°. Si tienen de 2 a 6 hélices son todas anfipáticas. Si tienen 7 o más hélices, alguna se sitúa en el centro o bien se disponen en dos o más capas. Pueden ser solubles o formar parte de membranas celulares. Ensamblados polihédricos (dominio de globina). Formados por hélices menos largas, con ángulos de ~ 20°, de ~ 50° o ambos en la misma proteína. A partir de 7 hélices, una ocupa la posición central o bien se organizan en dos o más capas. Proteínas beta.
- 2. De una sóla lámina (barril beta). Suelen tener 7 u 8 hebras, la primera enlazada por p de H con la última. El orden de las hebras no tiene porque reflejar su orden en la secuencia. La secuencia de las hebras presenta una marcada alternancia de residuos polares y apolares. Algunos barriles están abiertos y consisten en una lámina curva cuyo lado abierto lo tapa un bucle o alguna hélice. Hay barriles grandes de muchas más hebras que forman poros en membranas celulares. De varias láminas. Emparedados beta(`'beta sandwiches') . Consisten en dos láminas empaquetadas una contra la otra. Prismas beta. Consisten en tres láminas. Las láminas pueden orientarse paralela o perpendicularmente al eje ternario del prisma. Solenoides (hélices beta). Sucesión de hebras beta dispuestas helicoidalmente. A lo largo de la ‘hélice’, las hebras se enlazan para formas láminas beta. Turbinas (‘propellers’). Láminas beta, uno de cuyos laterales confluye hacia el centro de la proteína. Proteínas alfa/beta. Contienen hélices alfa y láminas beta (habitualmente paralelas). Las hélices y las hebras de la lámina se alternan a lo largo de la secuencia. Con lámina cerrada (barriles alfa/beta). Láminas de 7 u 8 hebras que forman un barril sobre cuya cara externa se empaquetan las hélices. Si hay más hebras, aparece un hueco central que se rellena con un bucle o una hélice. Las hebras son esencialmente apolares. Muchas son enzimas, en cuyo caso el sitio activo está en los bucles del lado carboxilo de las hebras. Con lámina abierta. Con frecuencia tienen menos de 7 hebras pero a veces tienen más. Casi siempre dan lugar a tres capas que suelen ser alfa/beta/alfa, aunque existen disposiciones de tipo beta/beta/alfa. A veces sólo hay dos capas (alfa/beta), como en las herradurasalfa/beta. Proteínas alfa+beta. Las hélices y las hebras de las láminas tienden a estar segregadas (no alternadas) en la secuencia. Las láminas tienden a ser antiparalelas. ¿Porqué? Pequeñas proteínas. Suelen tener menos de 60 aminoácidos. Son pobres en elementos de estructura secundaria. Su estructura tridimensional está frecuentemente estabilizada por puentes disulfuro o por cationes unidos . Concepto de dominio. Proteínas con varios dominios. Un dominio de plegamiento es una parte de una proteína cuyos residuos forman pocos contactos con el resto. Las proteínas descritas hasta ahora constan de un solo dominio. Muchas proteínas, sin embargo, tienen varios. Los dominios suelen conectarse en un solo punto. La estructura de cada dominio puede ser cualquiera de las descritas para proteínas monodominio. Genes que en un organismo dan lugar a varias proteínas pueden, en otro, estar fusionados y codificar una proteína multidominio. Ejemplos
- 3. Entre las proteínas globulares más conocidas tenemos la hemoglobina, un miembro de la familia de las globulinas. Otras proteínas globulares son las inmunoglobulinas (IgA, IgD, IgE, IgG e IgM), y las alfa, beta y gamma globulinas. Casi todas las enzimas con papeles importantes en el metabolismo son de forma globular, así como las proteínas implicadas en la transducción de señales en la célula. PROTEINAS GLOBULARES: las cadenas polipétidas se pliegan en forma esférica y poseen una esttructura más complejas que las anteriores, ya que puede haber más de una estructura secundaria en la misma molécula. Son solubles en agua . Algunas de las más importantes son: Mioglobina; interviene en el transporte y almacenamiento de oxigeno. Citocromo : es mitocondrias. componente de la cadena respiratoria en las Ribonucleasa: cataliza ciertos enlaces de ARN lisozima: cataliza la rotura hidrolítica de los polisacaridos . Albúminas: solubles en agua y coagulables por el calor y se encuentran en huevo, sangre leche y muchas plantas Globulinas: insolubles, existen en la leche, huevos y sangre y forma parte principal de las semillas. Proteína Mioglogina Citocromo c Lisozima RNA asa Quimotripsina Carboxipeptidasa nº residuos 153 104 129 124 247 307 % Hélice a 78 39 40 26 14 38 % Hoja b 0 0 12 35 45 17