Termodinámica: Procesos de vapor y gas en sistemas cerrados
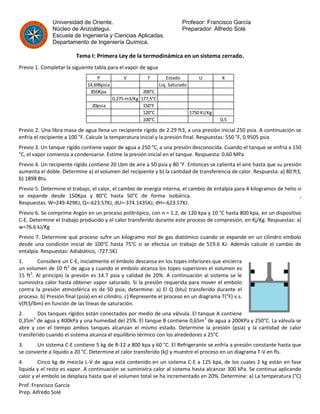
- 1. Prof. Francisco García Prep. Alfredo Solé Universidad de Oriente. Profesor: Francisco García Núcleo de Anzoátegui. Preparador: Alfredo Solé Escuela de Ingeniería y Ciencias Aplicadas. Departamento de Ingeniería Química. Tema I: Primera Ley de la termodinámica en un sistema cerrado. Previo 1. Completar la siguiente tabla para el vapor de agua Previo 2. Una libra masa de agua llena un recipiente rígido de 2.29 ft3, a una presión inicial 250 psia. A continuación se enfría el recipiente a 100 °F. Calcule la temperatura inicial y la presión final. Respuestas: 550 °F, 0.9505 psia Previo 3. Un tanque rígido contiene vapor de agua a 250 °C, a una presión desconocida. Cuando el tanque se enfría a 150 °C, el vapor comienza a condensarse. Estime la presión inicial en el tanque. Respuesta: 0.60 MPa Previo 4. Un recipiente rígido contiene 20 Lbm de aire a 50 psia y 80 °F. Entonces se calienta el aire hasta que su presión aumenta el doble. Determine a) el volumen del recipiente y b) la cantidad de transferencia de calor. Respuesta: a) 80 ft3, b) 1898 Btu Previo 5. Determine el trabajo, el calor, el cambio de energía interna, el cambio de entalpía para 4 kilogramos de helio si se expande desde 150Kpa y 80°C hasta 50°C de forma isobárica. , Respuestas: W=249.429KJ, Q=-623.57KJ, dU=-374.1435KJ, dH=-623.57KJ. Previo 6. Se comprime Argón en un proceso politrópico, con n = 1.2, de 120 kpa y 10 °C hasta 800 kpa, en un dispositivo C-E. Determine el trabajo producido y el calor transferido durante este proceso de compresión, en Kj/Kg. Respuestas: a) w=76.6 kJ/Kg Previo 7. Determine qué proceso sufre un kilogramo mol de gas diatómico cuando se expande en un cilindro embolo desde una condición inicial de 100°C hasta 75°C si se efectúa un trabajo de 519.6 KJ. Además calcule el cambio de entalpía. Respuestas: Adiabático, -727.5KJ 1. Considere un C-E, inicialmente el émbolo descansa en los topes inferiores que encierra un volumen de 10 ft3 de agua y cuando el embolo alcanza los topes superiores el volumen es 15 ft3 . Al principio la presión es 14.7 psia y calidad de 20%. A continuación al sistema se le suministra calor hasta obtener vapor saturado. Si la presión requerida para mover el embolo contra la presión atmosférica es de 50 psia; determine: a) El Q (btu) transferido durante el proceso. b) Presión final (psia) en el cilindro. c) Represente el proceso en un diagrama T(°F) v.s. V(ft3/lbm) en función de las líneas de saturación. 2. Dos tanques rígidos están conectados por medio de una válvula. El tanque A contiene 0,35m3 de agua y 400kPa y una humedad del 25%. El tanque B contiene 0,65m3 de agua a 200KPa y 250°C. La válvula se abre y con el tiempo ambos tanques alcanzan el mismo estado. Determine la presión (psia) y la cantidad de calor transferido cuando el sistema alcanza el equilibrio térmico con los alrededores a 25°C 3. Un sistema C-E contiene 5 kg de R-12 a 800 kpa y 60 °C. El Refrigerante se enfría a presión constante hasta que se convierte a líquido a 20 °C. Determine el calor transferido (kj) y muestre el proceso en un diagrama T-V en fls. 4. Cinco kg de mezcla L-V de agua está contenido en un sistema C-E a 125 kpa, de los cuales 2 kg están en fase liquida y el resto es vapor. A continuación se suministra calor al sistema hasta alcanzar 300 kPa. Se continua aplicando calor y el embolo se desplaza hasta que el volumen total se ha incrementado en 20%. Determine: a) La temperatura (°C) P V T Estado U X 14,696psia Liq. Saturado 850Kpa 200°C 0,275 m3/Kg 177,5°C 20psia 150°F 120°C 1750 KJ/Kg 100°C 0,5
- 2. Prof. Francisco García Prep. Alfredo Solé final. B) el trabajo (kJ) que se efectúa en el proceso descrito. C) El calor (kJ) transferido en el proceso. D) Mostrar el proceso en forma detallada en un diagrama P (kPa) v.s V(m3/kg) en fls. 2 kg están en fase liquida. 5. Un tanque rígido contiene 10 cc de agua líquida y 200 ml de vapor a 0.2 Mpa de presión abs. Luego se procede a un calentamiento hasta que la presión alcanza 10 Mpa. Muestre en un diagrama P(Mpa) v.s V (cm3/gr), en forma detallada, el proceso en fls. También, determine la cantidad de calor (kj) adicionado al proceso. Nota: Cualquier proceso energético expréselo en kJ. 6. Cinco kg de agua a 10°C y 700 kPa están contenidos en un sistema C-E, que tiene unos topes superiores e inferiores. Se suministra calor lentamente en agua, haciendo que el pistón se eleve hasta alcanzar los topes, en ese punto el volumen es 0.5 m3. Se continúa suministrando calor al agua hasta obtener solo vapor saturado. a) Determine la presión final (Mpa) dentro del cilindro, el trabajo (kJ) que se ha efectuado durante el proceso y el calor total absorbido (kJ). b) muestre el proceso en forma clara y detallada en un diagrama T-V en fls. 7. Se tiene una muestra de agua encapsulada a 1000 psia y 100 °F, ocupando un volumen de 0,3 pulgadas cubicas y está colocada en un recipiente cuyo volumen es un pie cubico. Por un vacío que se crea la capsula se rompe y el agua ocupa todo el recipiente. Si la temperatura se mantiene constante, determine el calor (BTU) que se transfiere. Nota: Los valores energéticos exprésalos en Btu/Lbm. Represente el proceso en un diagrama P-V en forma detallada en fls. 8. Un C-E contiene He inicialmente a 150 kpa, 20°C y 0.5 m3. El gas es comprimido en forma politrópica a 400 kpa y 140 °C. Determine el calor (kJ) transferido durante el proceso. Donde haga falta emplee R del gas. 9. Un sistema C-E contiene 0.005 m3 de agua líquida y 0.9m3 de agua en forma de vapor en condiciones de equilibrio a 600 kPa. Se le transfiere calor a presión ctte hasta que la temperatura alcanza 200 °C. Determine a) Temperatura (°C) inicial del agua, b) masa total (Kg) de agua, c) el volumen final (m3), d) muestre el proceso en un diagrama P-V en f.l.s. 10. Un dispositivo C-E vertical, de 12 cm de diámetro contiene un gas ideal a las condiciones ambiente: 1 bar y 24 °C. La cara interna del embolo está a 20 cm del fondo del cilindro. Entonces, un eje externo ejerce una fuerza sobre el embolo, que equivale a una entrada de trabajo de la frontera 0.1 kJ. La temperatura del gas permanece constante durante el proceso. Determine a) la cantidad de calor transferido, b) la presión en el cilindro y c) la distancia que se desplaza el embolo. 11. Dos tanques A y B está separados por un tabique. Inicialmente, el tanque A contiene 2 kg de vapor a 1 Mpa y 300°C, mientras que el tanque B contiene 3 kg de mezcla liquido-vapor saturado a 150 °C con una humedad de 50%. A continuación se quita el tabique y las dos partes se combinan hasta que se restablece el equilibrio mecánico y térmico. Si la presión del estado final es 300 kPa, determine: a) la temperatura final (°C) y la calidad (si existiera) en el estado final. B) la cantidad de calor (kj) transferido por los dos tanques. 12. Un envase aislado está dividido en 2 secciones A y B. La sección A contiene 2 kg de agua a 200 °C y 5 Mpa, la sección B con 0.985 kg a 200°C y 0.1 Mpa, se quita la división y el agua ocupa todo el envase. Determine: a Pfinal (MPA) y b) Q transferido 8kj) al mezclar las aguas si la T final es 200 °C. 13. En un sistema C-E hay agua a 300 kpa y 250°C. Se enfría el agua hasta tener vapor saturado y el embolo descansa sobre los topes. Se continúa el enfriamiento hasta 100 kpa. Determine ΔU total y muestre el proceso en f.d.l.f.l.s de T vs V. Además determine Q y W (kj/kg) 14. Parte a: Un kg de agua contenida en un C-E se vaporiza a 100°C. Si se adiciona 2236.9 kJ de calor. Calcule ΔU y ΔH (kJ) para el proceso mencionado 15. Un sistema C-E donde el embolo descansa sobre los topes contiene 2 kg de agua dentro de un volumen inicial de 0.02 m3. La Ti = 30°C. El embolo se despega de los topes a la presión de 1 Mpa. El agua se calienta desde su estado inicial hasta un estado final donde la temperatura final es 200 °C. Determine: a) El trabajo realizado por el embolo (kJ)
- 3. Prof. Francisco García Prep. Alfredo Solé b) El calor suministrado al sistema (kJ) c) Grafique en forma detallada en fls. d) Determine el volumen inicial ocupado por el líquido 16. Un tanque rígido contiene vapor de agua a 250 °C, a una presión desconocida. Cuando el tanque se enfría a 150 °C, el vapor comienza a condensarse. Estime la presión inicial en el tanque. 17. Parte A: Un gramo de nitrógeno contenido en un C-E es sometido a una secuencia de procesos cuasiestáticos, los cuales son: a) Una expansión adiabática doblándose el volumen b) Proceso isobárico en el cual el volumen se reduce al volumen inicial c) Compresión a V=ctte regresando al estado inicial. El N esta inicialmente a 150°C y 5 atm. Determine el trabajo (J) para cada proceso y el neto. Represente el proceso total en un diagrama P (Pa) vs. V (m3). Parte B: Manteniendo los procesos 1, 2, 3 arriba especificados, determine Q, W y ΔU para cada proceso si ahora se trabaja en forma irreversible con un rendimiento del 90%. R en J/Kg.K 18. Se condensa isotérmicamente vapor saturado a 200 °C hasta líquido saturado, en un dispositivo C-E. Calcule el calor transferido y el trabajo efectuado durante este proceso, en Kj/Kg. 19. Un kgmol de un gas diatómico, que se comporta idealmente, se calienta isométricamente desde 0°C hasta 50°C; y luego, isobáricamente hasta 100°C; a continuación ocurre una expansión y la temperatura se reduce hasta 75°C; finalmente se enfría isobáricamente hasta su estado original. El proceso completo significa una absorción de calor de 74,5 kCal por parte el sistema. Represente, lo expresado anteriormente, en un diagrama P-V. Además, calcule Q,W,ΔU, ΔH para cada una de las etapas y para todo el proceso. Especifique y demuestre que clase de proceso es la tercera etapa. Nota: Donde haga falta emplee R=1.987 kcal/kgmol.K. Resuelva el ejercicio empleando SOLO los valores dados. Los conceptos energéticos expréselos en kcal. Cv=(5/2)R 20. Un kg de aire contenido en un dispositivo C-E es sometido a una serie de procesos reversibles hasta completar un ciclo. La presión inicial es 0.5 Mpa y el volumen es 0.2 m3/kg durante el primer proceso el aire es expandido a presión constante. Luego se realiza una expansión sujeta a la expresión PV2=ctte hasta que la presión es 100 kpa y la temperatura es la misma que la temperatura inicial. A continuación el aire es comprimido a temperatura ctte hasta restaurar el estado inicial. Determine: a) W, Q, variación de en energía interna (kj). Para c/etapa y total b) Variación de entropía (kj/K). Para c/etapa y total c) Mostrar el proceso total en un diagrama P (MPA)- V(m3/kg), en forma detallada d) Determine la eficiencia del proceso, entendiendo por tal la relación entre el trabajo neto y el calor adicionado R= 0.2871 kj/kg.K 21. Aire cumple un ciclo a través de los siguientes procesos: 1-2 Isotérmico 2-3 Isométrico 3-4 Isobárico 4-1 Isentrópico a) Grafique el ciclo en diagramas P vs V b) Cuántos y cuáles procesos envuelven “Trabajo” c) Cuantos procesos y cuales implican “transferencia de calor” d) Determine el W (kj/kg) en el proceso 1-2, si se dobla el volumen Emplee R=0.2867 kj/kg.K 22. Un Kgmol de CO está sujeto a los siguientes procesos: Inicialmente el monóxido a 2.758 Mpa y 427 °C es expandido isotérmicamente hasta 0.552 Mpa. A continuación se hace un enfriamiento hasta 473.5 K isométricamente; se continua el enfriamiento hasta 77 °C a presión constante; luego se hace una compresión adiabática hasta 2,758 MPa y posteriormente un calentamiento a presión constante hasta los 700 K. Determine Q, W, ΔU, ΔH (kj) para c/e del proceso y global si se asume P.R. Grafique los procesos en un diagrama P(Mpa) v.s V (m3)
- 4. Prof. Francisco García Prep. Alfredo Solé 23. Calcular Q, W y variación de energía interna, en Btu, para cada una en las etapas (especificadas más abajo) y total cuando se dispone de 908 gmol de GI diatómico. Las etapas son: compresión isotérmica seguida de un calentamiento isobárico. Además, represente el proceso total en forma detalla en un diagrama P(atm) v.s V (ft3) Datos: P1= 1 atm, P2= 50 atm, T1 = 0 °C T2= 1000 °C 24. Un kilogramo mol de un G.I contenido en un recipiente cerrado con Cp= (5/2 R) y Cv= (3/2 R) cambia de P1 = 1 bar y V1 = 10 m3 hasta P2 = 10 bar y V2=1m3, mediante los siguientes procesos mecánicamente reversibles a) Compresión isotérmica b) Compresión adiabática seguida de enfriamiento a presión constante c) Calentamiento a volumen constante seguido de enfriamiento a presión constante Determine Q, W, variación de energía interna y entalpia para cada proceso y dibuje en un solo diagrama P-V la trayectoria de todos los procesos. 25. Una masa gaseosa se ajusta a las siguientes expresiones: PV= 85T y H=135 +0.9T. Encuentre los valores para Cp y Cv expresados en Btu/lbm°R. El Cp y Cv son dependientes únicamente de la temperatura. Nota: P(lbf/ft3) T(°R) V(ft3/lbm) H(Btu/lbm). Además, si los valores 85,135 y 0.9 tienen unidades, determínelos 26. Un recipiente rígido tiene una capacidad de 3ft3 . Contiene R-134a, en unas condiciones iniciales de 20°F y 74% de humedad. Calcule la cantidad de calor (BTU) necesaria para elevar la temperatura del sistema a 200°F. 27. Se tiene dióxido de carbono, el cual se comporta idealmente en un cilindro embolo durante su compresión de 0,3m3 hasta la mitad de su volumen. Durante este proceso la presión y el volumen se relacionan por la expresión donde a =8Kpa.m6 . Determine el trabajo empleado
