TENDENCIAS PERIÓDICAS
•
1 recomendación•623 vistas
Breve explicación.
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente

Enlace Químico. Ejercicios. Enlace Iónico y Enlace Covalente
Similar a TENDENCIAS PERIÓDICAS
Similar a TENDENCIAS PERIÓDICAS (20)
Último
Último (20)
6° SEM30 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

6° SEM30 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
LA ECUACIÓN DEL NÚMERO PI EN LOS JUEGOS OLÍMPICOS DE PARÍS. Por JAVIER SOLIS ...

LA ECUACIÓN DEL NÚMERO PI EN LOS JUEGOS OLÍMPICOS DE PARÍS. Por JAVIER SOLIS ...
Movimientos Precursores de La Independencia en Venezuela

Movimientos Precursores de La Independencia en Venezuela
PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx

PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx
la unidad de s sesion edussssssssssssssscacio fisca

la unidad de s sesion edussssssssssssssscacio fisca
Heinsohn Privacidad y Ciberseguridad para el sector educativo

Heinsohn Privacidad y Ciberseguridad para el sector educativo
TENDENCIAS PERIÓDICAS
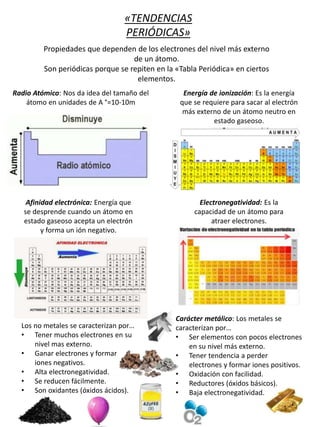
- 1. «TENDENCIAS PERIÓDICAS» Propiedades que dependen de los electrones del nivel más externo de un átomo. Son periódicas porque se repiten en la «Tabla Periódica» en ciertos elementos. Radio Atómico: Nos da idea del tamaño del átomo en unidades de A °=10-10m Energía de ionización: Es la energía que se requiere para sacar al electrón más externo de un átomo neutro en estado gaseoso. Afinidad electrónica: Energía que se desprende cuando un átomo en estado gaseoso acepta un electrón y forma un ión negativo. Electronegatividad: Es la capacidad de un átomo para atraer electrones. Carácter metálico: Los metales se caracterizan por… • Ser elementos con pocos electrones en su nivel más externo. • Tener tendencia a perder electrones y formar iones positivos. • Oxidación con facilidad. • Reductores (óxidos básicos). • Baja electronegatividad. Los no metales se caracterizan por… • Tener muchos electrones en su nivel mas externo. • Ganar electrones y formar iones negativos. • Alta electronegatividad. • Se reducen fácilmente. • Son oxidantes (óxidos ácidos).