Morfologia del musculo esqueletico
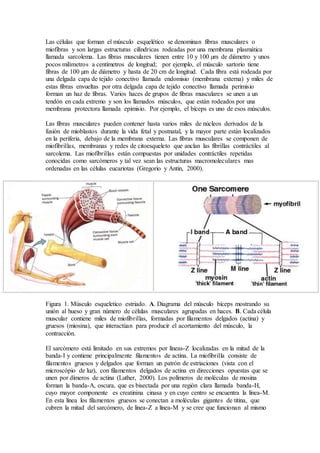
- 1. Las células que forman el músculo esquelético se denominan fibras musculares o miofibras y son largas estructuras cilíndricas rodeadas por una membrana plasmática llamada sarcolema. Las fibras musculares tienen entre 10 y 100 µm de diámetro y unos pocos milímetros a centímetros de longitud; por ejemplo, el músculo sartorio tiene fibras de 100 µm de diámetro y hasta de 20 cm de longitud. Cada fibra está rodeada por una delgada capa de tejido conectivo llamada endomisio (membrana externa) y miles de estas fibras envueltas por otra delgada capa de tejido conectivo llamada perimisio forman un haz de fibras. Varios haces de grupos de fibras musculares se unen a un tendón en cada extremo y son los llamados músculos, que están rodeados por una membrana protectora llamada epimisio. Por ejemplo, el bíceps es uno de esos músculos. Las fibras musculares pueden contener hasta varios miles de núcleos derivados de la fusión de mioblastos durante la vida fetal y postnatal, y la mayor parte están localizados en la periferia, debajo de la membrana externa. Las fibras musculares se componen de miofibrillas, membranas y redes de citoesqueleto que anclan las fibrillas contráctiles al sarcolema. Las miofibrillas están compuestas por unidades contráctiles repetidas conocidas como sarcómeros y tal vez sean las estructuras macromoleculares mas ordenadas en las células eucariotas (Gregorio y Antin, 2000). Figura 1. Músculo esqueletico estriado. A. Diagrama del músculo bíceps mostrando su unión al hueso y gran número de células musculares agrupadas en haces. B. Cada célula muscular contiene miles de miofibrillas, formadas por filamentos delgados (actina) y gruesos (miosina), que interactúan para producir el acortamiento del músculo, la contracción. El sarcómero está limitado en sus extremos por líneas-Z localizadas en la mitad de la banda-I y contiene principalmente filamentos de actina. La miofibrilla consiste de filamentos gruesos y delgados que forman un patrón de estriaciones (vista con el microscópio de luz), con filamentos delgados de actina en direcciones opuestas que se unen por dímeros de actina (Luther, 2000). Los polímeros de moléculas de mosina forman la banda-A, oscura, que es bisectada por una región clara llamada banda-H, cuyo mayor componente es creatinina cinasa y en cuyo centro se encuentra la línea-M. En esta línea los filamentos gruesos se conectan a moléculas gigantes de titina, que cubren la mitad del sarcómero, de línea-Z a línea-M y se cree que funcionan al mismo
- 2. tiempo como resorte y como regla para definir la longitud del sarcómero después de la contracción (Gautel et al., 1999). Los componentes primarios de las fibrillas de músculo esquelético son miosina y actina, así como tropomiosina y troponina asociadas con la actina. Otras proteinas musculares, como titina, neblina, α-actina y miomesina, son esenciales para regular el espaciamiento, unión y alineación precisa de los miofilamentos. Estas proteinas constituyen mas del 75% del total de proteinas de la fibra muscular. Figura 2. Mecanismo de la contracción muscular. A. Los filamentos delgados (actina) se deslizan sobre los filamentos gruesos (miosina) para producir el acortamiento del sarcómero. B. Diagrama de las moléculas de actina mostrando el sitio de la tropomiosina que se expone para la interacción con la actomiosina. En el músculo esquelético la distrofina del sarcolema se asocia a otras proteinas para formar un complejo que se cree une el citoesqueleto de actina a la matriz extracelular. La función y sobrevivencia de la miofibrilla dependen de esa unión, que estabiliza el sarcolema durante los ciclos repetidos de contracción y relajación, y trasmite la fuerza generada en los sarcómeros a la matriz extracelular (Petrof et al., 1993). Las integrinas (McDonald et al., 1995) y el complejo de glicoproteinas asociada a la distrofina (DGC) ayudan a mantener ese anclaje. Los componentes de la DGC se han descrito con detalle (Ohlendieck, 1996) y uno de sus componentes extracelulares, el β-distroglicano, proporciona un eslabón físico entre la matriz extrcelular y el citoesqueleto intracelular. La distribución precisa de la DGC en el sarcolema no se conoce, aunque la distrofina está concentrada en el sarcolema de las fibras de músculos esqueléticos en hilos orientados longitudinalmente y en las costámeras, que son regiones del sarcolema que se sobreponen a las líneas-Z y -M. Probablemente la proteina responsable de coordinar la distribución de proteinas en el sarcolema sea la misma actina (Williams y Bloch, 1999).
- 3. Figura 3. Proteinas estructurales del sistema de contracción del músculo. A. Diagrama de los componentes de un sarcómero, filamentos gruesos de miosina (azul) con la proteina titina para mantenerlos entre los filamentos delgados, y filamentos delgados de actina (rojo) con proteinas unidas (nebulina, tropomodulina, tropomiosina y troponinas. La distancia entre dos líneas-Z en reposo es alrededor de 2.5 µm. <http://www.bms.ed.ac.uk/research/others/smaciver/Myosin%20II.htm> B. Proteinas de la línea-Z, entre ellas actinina y vinculina. Las proteinas estructurales del citoesqueleto que sostienen los filamentos intermedios, como las proteinas vimentina, desmina y nestina, forman un eslabón físico que en los músculos estriados conecta las subunidades contráctiles al sarcolema. Estos filamentos pueden tener un papel importante en la organización celular durante la miogénesis, así como en mantener la integridad estructural de las miofibras maduras, redistribuyendo el estrés producido por la actividad contráctil (Vaittinen et al., 1999). En miofibras maduras la expresión de vimentina es completamente 'down'-regulada, mientras que la nestina, adyacente a la NMJ y la MTJ, se expresa a bajos niveles. A lo largo de la maduración la expresión de desmina aumenta contínuamente y finalmente se acumula en las márgenes de las líneas-Z, manteniendolas juntas a la membrana plasmática (Lazarides, 1980; Tkuyasu et al., 1985). A. Compartimentos membranales La superficie de la fibra muscular consiste de una membrana plasmática (sarcolema) y el sistema tubular-T, que aunque se contínuan, tienen una composición proteínica y lipídica diferente. La membrana plasmática de la miofibra también tiene dos tipos de áreas especializadas, la placa neuromuscular (neuromuscular junction, NMJ) y la unión con el tendón (myotendon junction, MTJ). 1. El sarcolema El sarcolema o membrana celular rodea el sarcoplasma o citoplasma de la fibra muscular y como otras membranas celulares, puede mantener un potencial a través de ella debido a la diferencia en la concentración de cargas positivas y negativas en el
- 4. interior y exterior de la célula. El primer paso en el proceso que lleva a la contracción es un cambio brusco en el potencial transmembrana, llamado potencial de acción. Otra característica notable del sarcolema es que tiene numerosas caveolas, consideradas como un tipo especializado de regiones lipídicas llamadas 'balsas', que contienen la proteina caveolina-3, específica del músculo. En el músculo esquelético diferenciado la caveolina-3 se asocia con los túbulos-T en desarrollo, pero en el músculo maduro está restringida a las caveolas del sarcolema y ya no es detectable en las túbulos-T (Payton et al., 1997). La localización exacta de caveolina-3 respecto a marcadores definidos de superficie ha sido estudiada por Rahkila y colaboradores (2001), quienes encontraron que el sarcolema del músculo parece ser un arreglo de áreas con balsas asociadas con caveolina y áreas sin balsas, que forman un mosaico de dominios de túbulos-T, vacuolas sarcolemales y dominios de β-distroglicanos. 2. El retículo sarcoplásmico Donde un túbulo transverso encuentra una miofibrilla, el túbulo es rodeado de cerca por la membrana del retículo sarcoplásmico (RS). Este es un complejo membranal similar al retículo endoplásmico en otras células, pero en el músculo esquelético forma una red tubular alrededor de cada miofibrilla. A cada lado del túbulo-T el retículo sarcoplásmico se ensancha y forma una cámara llamada cisterna terminal, que se une al túbulo-T por medio de una estructura conocida como 'pie'. La combinación de un par de cisternas terminales y el tubulo transverso se denomina 'triada' y aunque sus membranas están unidas, los contenidos líquidos están separados y son diferentes. La concentración intracelular de iones calcio (Ca2+) se mantiene baja debido a 'bombas', que los sacan cuando su concentración aumenta. Aunque las fibras de músculo esquelético 'bombean' Ca2+ hacia afuera de la célula, también eliminan el calcio del sarcoplasma transportándolo a la cisterna terminal del retículo sarcoplásmico. El sarcoplasma de una fibra muscular en reposo contiene concentraciones de Ca2+ alrededor de 10-7 molar/litro y su concentración dentro de la cisterna terminal puede ser hasta 1000 veces mayor; además, la cisterna contiene una proteina llamada calsecuestrina, que une los iones calcio en forma reversible. Incluyendo tanto el calcio libre como el calcio unido a otras moléculas, la concentración total de Ca2+ dentro de la cisterna puede ser hasta 40,000 veces la del interior del sarcoplasma que la rodea. Para que ocurra la interacción entre la actina y la miosina que produce la contracción, debe haber calcio, que después de la contracción debe ser eliminado y la entrega y eliminación de este ión se lleva a cabo por el trabajo combinado del sistema tubular-T y el RS. El RS rodea las miofibrillas como un sistema de redes, una de ellas alrededor de la banda-A y otra en la banda-I, y donde las dos redes se encuentran, en la unión de las bandas-A e -I, el RS forma una cisterna. El RS controla el nivel de Ca2+ intracelular en el músculo esquelético, almacenándolo y liberándolo. Inicialmente el retículo sarcoplásmico se desarrolla como un retículo endoplásmico, pero conforme el músculo se diferencía se enriquece con proteinas específicas (Volpe et al., 1992; Villa et al., 1993). Tres proteinas purificadas inicialmente del retículo sarcoplásmico son, la ATPasa de calcio (SERCA), calsecuestrina (CLQ) y el receptor a la rianodina (RyR). SERCA es responsable de bombear calcio hacia la luz del RS durante la relajación, mientras CLQ es la mas prominente de las proteinas intraluminales quelantes de calcio y entre ambas aumentan la capacidad del RS para el calcio. La proteina del SR mas abundante fuera de
- 5. la unión túbulo-T-RS es SERCA, que normalmente está distribuída en elementos tubulares rodeando la línea-Z y -M, así como en los elementos alineados con el eje longitudinal de la miofibrilla (Williams y Bloh, 1999). En la luz del RS la proteina mas abundante es CLQ (Jorgensen et al., 1977), un proteína ácida que une el calcio con afinidad moderada y alta capacidad. El extremo carboxilo de la CLQ es ácido y se une en forma específica al RS de la unión (Nori et al., 1993), donde CLQ y RyR están acopladas en forma funcional. La triadina es otra proteina de membrana, abundante en el RS de la unión, donde se colocaliza con RyR y ancla la CLQ a la cara membranal que enfrenta la unión, mediando el acoplamiento funcional entre el RyR y la CLQ en la luz del RS (Franzini-Armstrong et al., 1987; Guo y Campbell, 1995). La contracción muscular se inicia cuando los iones calcio almacenados en el retículo sarcoplásmico son liberados, difunden y entran en contacto con las unidades contráctiles individuales, las miofibrillas. 3. El sistema tubular transverso (STT) Una fibra muscular esquelética puede ser muy larga, hasta de varios centímetros de longitud, pero todas sus regiones deben contraerse simultáneamente, por lo que la señal que inicia la contracción debe distribuirse rápidamente a lo largo y hacia el interior de la célula. Para ello, la señal es propagada primero a lo largo del sarcolema y después conducida por los túbulos transversos o túbulos-T, que son tubos estrechos contínuos con el sarcolema que se extienen en ángulos rectos a la superficie celular. Los túbulos-T están llenos de líquido exracelular y forman vías dentro de la fibra muscular. Como su membrana tiene las mismas propiedades generales que el sarcolema, los potenciales de acción son conducidos hasta llegar a la región de las triadas, donde se inicia el proceso que acopla la excitación con la contracción. Aunque esta función de propagar rápidamente los potenciales de acción en la membrana superficial es la mejor conocida, los túbulos-T también pueden ser utilizados para llevar componentes del líquido extracelular al interior de las fibras musculares. Los túbulos-T forman una red contínua que corre transversalmente por varias miofibrillas y las penetra a todos los niveles, siendo sistemas de membranas conectadas con el sarcolema que mantienen una composición de lípidos y proteinas diferente a la del sarcolema (Flucher, 1992; Parton et al., 1997). Algunos estudios han proporcionado evidencias de que se originan como un compartimento tubular interno que después se funde con la membrana del sarcolema (Flucher et al., 1993), aunque en otros estudios se dice que se forman por la fusión repetida de caveolas, ayudadas por amphyphysina (Lee et al., 2002). La caveolina-3, específica de músculo, puede ser requerida para generar la composición única de proteinas y lípidos del sistema tubular-T (Parton et al., 1997) y la amphiphysina II es esencial para su organización y morfología normal. La amphiphysina II se colocaliza con la ankyrina y tiene un papel en anclar la ramificación de los túbulos y en organizar sus componentes proteicos (Razzaq et al. 2001). Se ha encontrado que las isoformas de ankyrina-1 se localizan en la línea-M, donde se unen a oscurina, una interaccíon que puede proporcionar un eslabón directo entre el RS y las miofibrillas (Bagnato et al., 2003).
- 6. Figura 4. A. Diagrama del reticulo sarcoplásmico, mostrando las cisternas terminales y su relación cercana con los túbulos transversos (morado). B. Ciclo que inicia la contracción; a la izquierda está la terminal nerviosa, que al liberar acetilcolina induce un potencial de acción que viaja por la membrana superficial(flechas) e ingresa a los túbulos transversos. Ahí estimula la liberación de calcio por parte del retículo sarcoplásmico (verde) y este catión difunde a los miofilamentos para producir su interacción y la contracción de la fibra muscular. Los túbulos-T están localizados entre la cisterna terminal adyacente al RS, formando una triada compuesta por dos cisternas terminales y el túbulo-T. Las uniones RS-túbulo- T y sus asociaciones con miofibrillas se desarrollan en una serie de pasos consecutivos (Flucher, 1992; Flucher et al., 1993), donde la formación de uniones entre los dos sistemas membranales se hace en forma concurrente, iniciando cambios moleculares en ambos sistemas de membranas (Takekura et al., 2000). Cuando el potencial de acción nervioso llega a la membrana muscular, esta sufre una depolarización que es trasmitida a las profundidades de la célula por las membranas del sistema tubular-T. Cuando el potencial de acción de los túbulos es detectado por un receptor a la dihidropiridina localizado en la unión del túbulo con la cisterna del retículo sarcoplásmico, un mecanismo aún no dilucidado produce la apertura de los receptores a la rianodina, que funcionan como canales para el calcio. Cuando estos canales se abren, como la concentración de iones calcio dentro del RS es mucho mayor que en citosol de la célula, estos iones salen de su depósito para iniciar el proceso de la interacción entre los filamentos gruesos y delgados, la contracción muscular. Esta serie de eventos es llamada el 'acoplamiento excitación-contracción' (e-c) y varias proteinas específicamente localizadas en la unión RS-túbulo-T tienen papeles esenciales
- 7. en ellos. El receptor a la dihidropiridina (DHPR) en el túbulo-T detecta el voltaje a través de la membrana y su activación produce la liberación de Ca2+ del RS (Flucher, 1992), mientras el canal de liberación RyR/Ca2+ está localizado en el RS de la unión y es responsable de la liberación de Ca2+ de sus lugares de almacenamiento. Tanto el RyR como el DHPR son necesarios para el desarrollado apropiado del músculo, aunque ninguno de ellos lo es para el anclaje T-RS o la búsqueda y/o asociación de CLQ y tradina en el RS de unión (Felder y Franzini-Armstrong, 2002). B. El aparato contráctil 1. Los sarcómeros Las miofibrillas son haces de filamentos gruesos y delgados organizados en unidades funcionales repetitivas llamadas sarcómeros y como en reposo cada uno de ellos tiene una longitud de 1.6-2.6 µm, una miofibrilla tiene aproximadamente 10,000 sarcómeros de un extremo a otro. Los sarcómeros son las unidades funcionales mas pequeñas de la fibra muscular y cada uno de ellos contiene filamentos gruesos, filamentos delgados, proteinas que estabilizan la posición de los filamentos y proteinas que regulan las interacciones entre los filamentos delgados y gruesos. Las interacciones entre los filamentos gruesos y delgados de los sarcómeros son las responsables de la contracción muscular. La apariencia estriada de cada miofibrilla se debe a las diferencias en tamaño, densidad y distribución de los filamentos gruesos y delgados. La estriación se forma alternando bandas oscuras (bandas-A) y claras (bandas-I), cuyos nombres derivan de las palabras anisotrópico e isotrópico y se refieren a la apariencia de las bandas cuando son vistas con un microscopio de luz polarizada. Figura 4. Diagrama animado del arreglo de miofibrillas en un músculo estriado en reposo y su cambio durante la contracción. a. La banda-A Los filamentos gruesos están colocados en el centro del sarcómero, en la banda-A, cuya longitud es igual a la longitud de un filamento grueso típico. Sin embargo, la banda-A también incluye porciones de los filamentos delgados y tiene tres subdivisiones: 1. La línea-M. La porción central de cada filamento grueso se conecta con sus vecinos por medio de proteinas en la línea-M, que ayudan a estabilizar sus posiciones.
- 8. 2. La zona-H. En un sarcómero en reposo, la zona-H o banda-H es una región mas clara a cada lado de la línea-M y contiene filamentos gruesos pero no filamentos delgados. 3. La zona de sobreposición. En esta zona los filamentos delgados están situados entre los filamentos gruesos, de manera que cada filamento delgado está rodeado por tres filamentos gruesos y cada filamento grueso por seis filamentos delgados. b. La banda-I Cada banda-I se extiende desde la banda-A de un sarcómero hasta la banda-A del siguiente sarcómero y contiene filamentos delgados, pero no filamentos gruesos, con las líneas-Z marcando la frontera entre sarcómeros adyacentes. Estas líneas-Z consisten de proteinas llamadas 'conectinas', que interconectan los filamentos delgados de sarcómeros adyacentes. Desde las líneas-Z en el extremo de cada sarcómero, los filamentos delgados se extienden en la zona de sobreposición hacia la línea-M. Hilos de una proteina llamada 'titina' se extienden desde la punta de los filamentos gruesos a los sitios de unión en la línea-Z y ayudan a la fibra muscular a resistir el estiramiento, que en otra forma trastornaría el arreglo de miofibrillas y el mecanismo de la contracción. Cada sarcómero está rodeado por dos túbulos transversos y las triadas se localizan a ambos lados de la línea-M, en la zona de sobreposición. Como resultado, los iones calcio liberados por el retículo sarcoplásmico entran en las regiones donde los filamentos delgados y gruesos interactúan. Cada línea-Z está rodeada por una red de filamentos intermedios que interconectan miofibrillas adyacentes y las mas cercanas al sarcolema se unen a sitios específicos en el interior de la membrana. Debido a que las líneas-Z de todas las miofibrillas están alineadas, la fibra muscular como un todo tiene una apariencia estriada, que como es visible al microscópio de luz da al músculo esquelético su aparencia y clasificación de estriado. Ahora consideraremos la estructura molecular de los filamentos responsables de la contracción muscular. 2. Los filamentos delgados Un filamento delgado típico tiene 5-6 nm de diámetro y 1 µm de longitud, y está formado por cuatro proteinas, actina-F, nebulina, tropomiosina y troponina. La actina-F es un hilo torcido compuesto por dos hilos de 300-400 moléculas globulares individuales de actina-G. Un hilo largo de nebulina es una espiral que se coloca a lo largo del filamento de actina-F en el espacio entre los hilos de moléculas de actina-G y mantiene juntos los hilos de actina-F. Conforme los filamentos delgados se desarrollan, probablemente la longitud de la molécula de nebulina determina la longitud del hilo de actina-F. Cada molécula de actina-G contiene un sitio activo que puede unirse a los filamentos gruesos, en la misma forma como una molécula de sustrato se une a los sitios activos de una enzima. En condiciones de reposo, el complejo troponina-tropomiosina evita la unión de la miosina.
- 9. Una molécula de tropomiosina es una proteina con dos hilos que cubre siete sitios activos y evita la interacción actina-miosina. En su región media está unida a una molécula de troponina. Una molécula de troponina consiste de tres subunidades globulares. Una subunidad se une a la tropomiosina, manteniéndola junta como complejo troponina-tropomiosina, mientras una segunda subunidad se une a la actina-G, manteniendo en posición el complejo troponina-tropomiosina. La tercera subunidad tiene un receptor que une el ion calcio, pero en un músculo en reposo las concentraciones intracelulares de Ca2+ son muy bajas, por lo que el sitio se encuentra vacío. Para que la contracción ocurra, la posición del complejo troponina-tropomiosina debe cambiar, exponiendo los sitios activos de la actina-F, un cambio en posición que ocurre cuando los iones Ca2+ se unen a receptores en las moléculas de troponina. En cada extremo del sarcómero los filamentos delgados se unen a la línea-Z y aunque es llamada línea porque se ve como una línea oscura en la superficie de la miofibrilla, en cortes de sección se ve como una red abierta, por lo que también se le llama disco-Z. 3. Los filamentos gruesos Los filamentos gruesos son de 10-12 nm de diámetro y 1.6 µm de longitud y cada uno de ellos consiste de aproximadamente 500 moléculas de miosina arregladas en un par de subunidades enrrolladas. La larga cola se une a otras moléculas de miosina en el filamento grueso, mientras la cabeza está libre y sobresale hacia el filamento delgado mas cercano; como durante la contracción interactúa con los filamentos delgados, se le llama también 'puente cruzado'. La conexión entre la cabeza y la cola funciona cono un gozne que permite a la cabeza pivotear en su base y cuando esto ocurre, se mueve hacia dentro o fuera de la línea-M. Este pivoteo es la clave de la contracción muscular. Todas las moléculas de miosina se arreglan con sus colas apuntando a la línea-M, pero la zona- H incluye una región central donde no hay cabezas de miosina, aunque en otras regiones las cabezas de miosina están arregladas en espiral, cada una enfrentando uno de los filamentos delgados que la rodea. Cada filamento grueso tiene un núcleo de la proteina titina. Así, a cada lado de la línea- M hay un hilo de titina que se extiende a través de toda la longitud del filamento grueso y continúa a través de la banda-I hasta la línea-Z de ese lado. Esa porción del hilo de titina expuesta en la banda-I es muy elástica y después del estiramiento recupera su longitud. A la longitud de reposo del sarcómero, los hilos de titina están completamente relajados y se tensan solamente cuando alguna fuerza externa alarga el sarcómero. C. Contracción muscular Los iones calcio en contacto con los miofilamentos inician la interacción de las proteinas que los forman, miosina y actina. En reposo estas proteinas tienen afinidad natural una or la otra, pero no se pueden poner en contacto porque otras dos proteinas, la troponina y la tropomiosina, se encuentran entrelazadas alrededor de ellas y lo evitan; sin embargo, cuando llega el Ca2+ la forma del complejo troponina-tropomiosina cambia y esto permite que la miosina y la actina se pongan en contacto.
- 10. Figura 5. A. La Troponina (Tn) como molécula interruptora miofibrilar Ca21, cuya organización troponina-tropomiosina-actina está de acuerdo con Gagné y cols. La TnC se muestra en azul para el dominio NH2 y rosa para el dominio COOH. TnI se muestra en rojo (dominio terminal-NH2), café (dominio terminal COOH) y amarillo (región inhibidora). TnT está en verde, la miosina en verde (miosina-S1), rojo (cadena ligera esencial) y amarillo (cadena ligera regulaadora) en la representación con palitos. La tropomiosina se muestra en azul ligero y azul oscuro. Notese que sólo la TnC, miosina y tropomiosina están representadas por su estructura conocida, mientras las estructuras de TnT y TnI son modelos. Los monomeros de actina están representados por esferas blancas. a. Organización del músculo en el estado relajado. El dominio COOH de TnC está unido a Mg21. El dominio de la terminal NH2 de TnI está anclado sobre el dominio COOH de TnC, mientras la región inhibitoria y el dominio de la terminal-COOH de TnI hacen contacto con la actina y la tropomiosina. Esta organización mantiene el filamento delgado en una conformación que evita que la miosina interactúe con la actina. b. Organización después que dos Ca21 se unen al dominio NH2 de TnC que, a su vez, interactúan con TnI. Entonces la región inhibitoria y el dominio COOH de TnI son liberados de la actina. Esto lleva a una conformación del filamento delgado que permite la formación adecuada del complejo actomiosina y ya puede ocurrir el 'paleo' (no mostrado aquí) que desliza en filamento delgado hacia la derecha. (Berchtold et al., 2000). B. Animación del movimiento que hacen las cabezas de miosina para deslizar el filamento delgado (hecho con actina, tropomiosina y troponina) sobre el grueso (hecho con miosina). Nótese que la cabeza sólo puede unirse al filamento delgado de actina (bolas color naranja) cuando el sitio de unión en la tropomiosina (filamento azul) es
- 11. expuesto por el movimiento del complejo de troponina (formado por tres subunidades, troponina-T (que se une a la tropomiosina), troponina-C (que es el sitio de unión para el Ca2+) y troponina-I (que inhibe [bloquea] el sitio de unión en la actina), facilitado por la unión del ión calcio (en realidad cuatro iones Ca2+) con la troponina-C. Después, el ATP proporciona la energía para que la cabeza se separe del filamento delgado y avance al siguiente punto de unión. La forma de la molécula de miosina es muy compleja, con un tallo largo que al final tiene cabezas globulares que se unen a su porción mayor. Una sola molécula de miosina tiene numerosas cabezas, que como son flexibles, permiten el movimiento en la longitud de la molécula de actina. Este movimiento puede ser visto un poco como el de una lancha con varios remos, que se desconectan del sitio de unión en la actina después de un golpe y regresan a su orientación original para unirse a otro sitio de unión un poco mas adelante del filamento de actina. Este proceso desliza el filamento de actina a lo largo del filamento de miosina, un mecanismo que se conoce como 'deslizamiento de los miofilamentos'. La energía para el deslizamiento de los filamentos proviene de las moléculas de ATP, pero también se requiere energía para detener el proceso de la contracción muscular. La contracción se detiene cuando el Ca2+ es eliminado de la inmediata vecindad de los miofilamentos, lo que ocurre porque la membrana del sistema retículo sarcoplásmico tiene 'bombas' que utilizan ATP para transportarlo a su interior. Cuando el calcio es eliminado, la troponina-tropomiosina recupera su posición inhibitoria entre las moléculas de actina y de miosina. Es importante indicar que todo eso ocurre en grupos de fibras musculares, que junto con un axón motor forman una unidad motora. Cuando se requiere la contracción muscular para un ejercicio, no se activan todas las unidades motoras y la mayor parte de los movimientos utlizan solamente una fracción de la potencia total del músculo. El sistema nervioso motor controla y gradúa la intensidad de la contracción muscular, 'reclutando' un número variable de unidades motoras y es posible que incluso durante las contracciones que producen un acortamiento máximo del músculo, no se recluten todas las unidades motoras. En esta página hemos simplificado la descripción de los eventos que llevan a la contracción del músculo esquelético y hay otras proteinas involucradas que no sólo se conocen bien, sino que tienen importancia médica porque sus alteraciones resultan en enfermedades musculares bien conocidas (i.e., distrofia muscular). Por ello las hemos colocado en una sección diferente que puede encontrarse aquí. D. Aprovisionamiento de energía Las células no almacenan grandes cantidades de ATP porque una vez que se inicia la contracción muscular lo pueden generar muy rápidamente. Hay tres fuentes primarias del ATP que, en órden de utilización, son: el fosfato de creatinina (creatine phosphate, CP), la glicólisis anaeróbica y la fosforilación oxidativa. La energía deriva de la ruptura de la unión del fosfato terminal de la molécula de ATP, que entonces queda como ADP (difosfato de adenosina). El fosfato de creatinina convierte el ADP en ATP, donando un fosfato en presencia de la enzima creatinina-
- 12. cinasa (creatine kinase, CK) o creatina-fosfocinasa (creatine phosphokinase, CPK). La reacción de la CP con el ADP para formar ATP es muy rápida, pero este no dura mucho tiempo porque la célula no almacena grandes cantidades de CP; sin embargo, durante contraccioness cortas de gran intensidad la CP sirve como la mayor fuente de energía. Esta forma de generación de energía es llamada aláctica anaeróbica, porque no produce lactato ni requiere oxígeno y es de gran importancia durante los deportes que requieren explosiones de potencia, como la carrera de 100 metros planos. Figura 7. Esquema de los mecanismos bioquímicos del músculo para la obtención de energía. A. Músculo en reposo. B. Músculo durante una contracción. Tan pronto como se inicia la contracción también empieza el proceso de glicólisis, llamado anaeróbico porque no requiere oxígeno y aunque en el corto plazo no proporciona tanta energía como el CP, su contribución puede durar unos 30-60 segundos. El sustrato para la generación de energía durante la glicólisis es proporcionado por el glicógeno almacenado en el músculo y posiblemente por algo de glucosa sanguínea. Como producto final de la glicólisis anaeróbica pura se forma ácido láctico y si se forma mucho, puede bajar el pH de la célula hasta el punto en que se detenga en metabolismo. El mayor sustrato para la glicólisis anaeróbica es el glicógeno, de manera que para no limitar los músculos a un trabajo intenso pero de poca duración, después de un ejercicio intenso y antes de otro se requiere del almacenamiento de glicógeno. La virtualmente infinita cantidad de energía proviene del proceso de fosforilación oxidativa, aunque las cantidades de energía que produce este proceso no son tan altas como las de la glicolisis, por lo que los eventos aeróbicos como el maratón se corren a
- 13. un paso considerablemente mas lento que los 400 metros planos. Los sustratos para el metabolismo oxidativo son principalmente la glucosa y las grasas (ácidos grasos libres, no colesterol), aunque las proteinas también pueden ser fuente de energía por medio de conversiones intermedias a glucosa, precursores de la glucosa o ácidos grasos libres. Como la grasa puede metabolizarse aeróbicamene, la mayor parte de los humanos bien nutridos tienen un aprovisionamiento virtualmente infinito de energía para el ejercicio de baja intensidad y la limitación en estos casos se debe a una disminución del sustrato, aunque la deplesión del glicógeno muscular también puede resultar en fatiga durante los eventos aeróbicos. E. Unidad motora Cada fibra muscular es controlada por el cerebro por medio de un nervio motor y contribuye a la produción de fuerza. Un nervio motor puede tener decenas, cientos y aún miles de ramificaciones que terminan en fibras musculares diferentes y junto con todas las que inerva, constituyen una unidad motora. Por ejemplo, el músculo recto anterior del muslo, uno de los cuatro músculos que forman el cuadríceps, puede contener hasta 1 millón de fibras musculares controladas por alrededor de 1,000 nervios motores, lo que en promedio corresponde a alrededor de 1,000 fibras musculares en cada unidad motora. Figura 8. Diagrama ilustrando unidades motoras. a. Una sola unidad motora, formada por una motoneurona y cinco fibras musculares. b. Dos unidades motoras; una con cuatro fibras musculares (verde) y otra con tres fibras (morado). Figura 9. Una unidad motora de músculo esquelético formada por una motoneurona (con tres ramas axónicas) y tres fibras musculares. El tipo de fibras musculares que forman una unidad motora siempre es homogéneo, por lo que consiste totalmente en fibras de tipo I (sacudida lenta) o fibras de tipo II (sacudida rápida). Sin embargo, como cada músculo tiene una combinación de unidades motoras lentas y rápidas, la composición del músculo completo es heterogénea.
- 14. F. Unión neuromuscular Un músculo es controlado por una motoneurona, cuyo axón llega a la región llamada sinápsis, donde ambas células se acercan a una distancia de aproximadamente 200 nm. Cuando la motoneurona se activa manda un impulso eléctrico (potencial de acción) a lo largo del axón, que en su extremo libera una molécula llamada neurotrasmisor, la acetilcolina. Cada miofibrilla está inervada por el axón de las neuronas motoras de la médula espinal o del tallo cerebral y responde a la llegada de potenciales de acción. Una sola motoneurona puede hacer contaco con decenas y hasta miles de miofibrillas, pero en los humanos cada una de ellas está inervada por sólo el axón terminal de una neurona. La estructura especializada en el sitio de contacto entre las ramas terminales del axón y el músculo se llama placa motora o unión neuromuscular (neuromuscular junction, NMJ) y ahí la membrana tiene profundos pliegues que aumentan el área receptora (Ishikawa y Shimada, 1982). Generalmente la NMJ está localizada en el tercio medio de la miofibra. Las fibras nerviosas no solamente indican a las células musculares el momento de la contracción, sino que también ejercen una influencia trófica sobre ellas, lo que es necesario para mantener su integridad estructural. La característica de la NMJ es su alta concentración de receptores a la acetilcolina y de varias proteinas asociadas, así como de las mRNAs que las codifican (Ralston et al., 1997). Figura 9. Diagrama de la sinapsis, llamada placa neuromuscular, entre un nervio y un músculo. A. Diagrama de la inervación del axón. B. Zona de acercamiento (placa neuromuscular) entre el axón y el músculo. C. Microfotografía de dos placas neuromusculares. La acetilcolina liberada en la terminal nerviosa se une a receptores específicos en la membrana de la célula muscular y esto inicia un potencial de acción en el músculo. Poco después una enzima, la acetilcolinesterasa, descompone la acetilcolina para terminar la influencia nerviosa, ya que el músculo solamente genera un potencial de acción cada vez que el nervio es activado.
- 15. Una vez que la membrana muscular ha sido excitada genera su propia corriente eléctrica para producir un potencial de acción muscular, que no solamente se propaga a lo largo de la fibra, sino que también penetra en su interior viajando en el sistema tubular-T. Cuando el potencial de acción pasa por las regiones donde estos túbulos enfrentan la cisterna del sistema retículo sarcoplásmico se produce la liberación de iones calcio, que al ponerse en contacto con la maquinaria contráctil inician la contracción muscular G. Unión músculo-tendón La unión músculo-tendón (MTJ) es una interface entre el músculo y el tendón, morfológicamente especializada para trasmitir al tendón las fuerzas contráctiles generadas por las miofibrillas activas. En esta región la fibra muscular termina abruptamente, aguzándose y mandando proyecciones citoplásmicas longitudinales e invaginaciones como dedos que se entrelazan con las fibras de colágeno del tendón. Esas prolongaciones y pliegues aumentan el área de la interface al menos por un órden de magnitud sobre el área de sección de la fibra muscular y también aseguran que el estrés aplicado a la interface ocurra principalmente como 'rozamiento' (Williams et al., 1980). Estructuralmente, la MTJ tiene varios componentes, filamentos de actina que se extienden desde la última banda-A, proteinas que unen los haces de filamentos de actina al sarcolema, proteinas transmembranales que se unen a componentes extracelulares, la lámina exerna y otras proteinas que la unen a la matriz rica en fibrillas de colágeno fuera de ella. Las evidencias apoyan el punto de vista de que las fibras del músculo esquelético tienen dos sistemas paralelos para unir las proteinas estructurales intra- y extracelulares, el sistema distrofina-DPG (Bao et al., 1993) y el sistema de integrinas α- 7 β-1 (Trotter, 2002). Sin embargo, también la desmina puede trasmitir fuerza desde los generadores de fuerza miofibrilares a la superficie muscular y al MTJ (Lieber et al., 2002). H. Regulación de la fuerza muscular Para regular la fuerza que produce un solo músculo el cerebro combina dos mecanismos de control, el reclutamiento y la frecuencia de activación. En el primer caso, las unidades motoras que forman un músculo no se reclutan al azar, sino de acuerdo a su tamaño; esto es, las unidades musculares pequeñas (pocas fibras musculares) son inervadas por motoneuronas pequeñas y tienen un umbral de activación bajo, de manera que son reclutadas primero. Después, conforme un ejercicio requiere mas fuerza se reclutan las unidades motoras mas grandes y esto tiene un gran significado funcional, porque cuando el requerimiento de fuerza es bajo pero la demanda de control es alta (como al escribir, tocar el piano, etc.), el reclutamiento de sólo unas pocas fibras musculares proporciona la posibilidad de un control fino. En cambio, cuando se necesita mas fuerza, la contribución de cada unidad motora a la producción total de fuerza se hace mayor. También es importante saber que las unidades motoras pequeñas son generalmente unidades lentas, mientras las unidades motoras grandes están compuestas de fibras de sacudida rápida. El segundo mecanismo de regulación de la fuerza es la frecuencia de generación de los potentiales de acción por parte de la motoneurona y una unidad motora tiene un gran espectro de frecuencias. Las unidades lentas operan en un intervalo de frecuencia mas
- 16. bajo que las unidades mas rápidas y dentro de ese intervalo, la fuerza generada por una unidad motora aumenta con el aumento en la frecuencia de disparo. Así, cuando un potencial de acción nervioso llega a la fibra muscular antes que esta se haya relajado completamente de la contracción previa, se produce una suma en la fuerza de contracción. Por medio de este mecanismo la frecuencia de disparo de la motoneurona afecta la fuerza muscular generada por cada unidad motora. Figura 10. Diagrama ilustrando el reclutamiento de unidades motoras dependiendo de la fuerza requerida para hacer un ejercicio. Si el ejercicio sólo requiere una intensidad débil se reclutan unidades motoras tipo I (sacudida lenta), pero si se aumenta la intensidad del ejercicio se reclutarán además unidades tipo IIa (sacudida rápida). Si se requiriera todavía mayor intensidad se reclutarán unidades tipo IIb, que ayudarán a las unidades tipo IIa y tipo I. Por lo tanto, las unidades tipo I estarán siempre activadas durante un ejercicio, sin importar su intensidad. Las relaciones entre el patrón de disparo de la motoneurona y la intensidad del ejercicio son tales, que durante un ejercicio de baja intensidad, como caminar o correr lentamente, se utilizan selectivamente las fibras de sacudida lenta porque tienen un umbral mas bajo para el reclutamiento. Sin embargo, si bruscamente aumentamos el paso hasta llegar a la carrera, se reclutan las unidades rápidas mas grandes. En general, conforme aumenta la intensidad del ejercicio en cualquier músculo, aumenta la contribución de las fibras rápidas. Para un músculo la intensidad del ejercicio se traduce en fuerza por contracción y frecuencia de contracciones por minuto, y el reclutamiento de las unidades motoras se regula por la fuerza requerida. En un músculo que ha estado en reposo se recluta el número de unidades motoras suficiente para proporcionar la fuerza requerida, lo que
- 17. inicialmente puede ser obtenido con pocas o ninguna unidad motora rápida. Sin embargo, conforme las unidades lentas se fatigan y dejan de producir fuerza, el sistema nervioso trata de mantener la fuerza requerida reclutando las unidades rápidas. Como la misma producción de fuerza en un músculo fatigado requiere mas unidades motoras, se reclutan las unidades motoras rápidas, fatigables. Así, debido al aumento en el lactato producido por el reclutamiento tardío de unidades rápidas, la fatiga se acelera hacia el final de periodos largos o severos de ejercicio. I. Fibras musculares 1. Tipos Aunque todas las miofibras esqueléticas tienen la misma organización básica, usando criterios estructurales, contráctiles y metabólicos, así como sus patrones expresión genética, se pueden describir dos tipos de fibras, que se clasifican como de sacudida lenta o rápida (Hughes, 1998). Las fibras oxidativas, rojas y de sacudida lenta (tipo I), están involucradas en eventos contráctiles tónicos, sostenidos y mantienen una concentración de Ca2+ en niveles relativamenta altos (100-300 mM). En contraste, las fibras glicolíticas, blancas y de sacudida rápida (tipo II), se usan para descargas de contracciones bruscas y se caracterizan por transientes de Ca2+ breves y de gran amplitud, con bajos niveles de Ca2+ (<50 nM). Las propiedades de las fibras musculares esqueléticas dependen del patrón de estimulación neuronal, de manera que una gran actividad de las motoneuronas tónicas promueve el fenotipo de fibras lentas, mientras las descargas poco frecuentes de las motoneuronas resultan en fibras rápidas (Olson y Williams, 2000). Cuando se compara la estructura de las miofibras de tipo II con las de tipo I, estas tienden a ser mas estrechas, con bandas Z y M mas anchas, tienen mas glicógeno y su sarcoplasma es mas rico en mitocondrias. La base molecular para la diversidad funcional de las miofibras es la expresión de isoformas específicas de la mayor parte de las proteinas involucradas en la contracción y relajación muscular. La clasificación de las miofibras está basada en la velocidad de contracción y otras propiedades fisiológicas, pero está de acuerdo principalmente con las isoformas específicas de la miosina de cadena pesada (MyHCl; Schaffino y Reggiano, 1996; Halston et al., 2001). Los detalles morfológicos varían en diferentes fibras musculares y los músculos esqueléticos responden a cambios en las demandas fisiológicas remodelando la arquitectura de las fibras individuales. Cuando los músculos se mantiene a longitudes anormalmente largas o cortas, se añaden o eliminan sarcómeros y cuando las fibras musculares funcionan contra cargas anormalmente pesadas o ligeras, se añaden o eliminan filamentos (Trotter, 2002), lo que lleva a cambios en la masa de tejido. También pueden cambiar las relaciones espaciales entre las células musculares y otros componentes del tejido y la expresión genética puede ser reprogramada para alterar las propiedades metabólicas y contráctiles especializadas de las miofibrillas (Olson y Willims, 2000). No todas las fibras que componen los músculos esqueléticos son iguales y cuando se estimulan en forma repetida, algunas son mas resistentes que otras (fatiga se refiere a una disminución en la fuerza generada por el músculo o la unidad motora cuando se estimula). Además, las unidades motoras resistentes a la fatiga tienden a contraerse en
- 18. forma mas bien lenta, comparadas con aquellas que se fatigan mas rápidamente. Así, las fibras musculares lentas se fatigan rápidamente y tienen sacudidadas lentas, mientras las fibras musculares rápidas se fatigan rápidamente y tienen sacudidas rápidas, lo que se muestra en la Figura X. Figura 11. Diferencias relativas en la duración de una sacudida simple y la fuerza generada por fibras musculares rápidas y lentas. 2. Clasificación histórica La clasificación de las fibras musculares no es tan simple como se ilustra en la Figura X, ya que sus propiedades funcionales, desarrollo de fuerza máxima, velocidad de contracción, resistencia a la fatiga, capacidades oxidativas y glocolíticas, y actividades ATPásicas de la actina-miosina, caen en un amplio espectro. Sin embargo, a pesar de esa complejidad es posible dividirlas en pocos grupos. Así, basados en las propiedades contráctiles de las unidades motoras (fuerza, velocidad y fatigabilidad), Burke y colaboradores (1973) las separaron en cuatro tipos; además, algunas pruebas histoquímicas permitieron identificar cuatro tipos de fibras que parecían correlacionarse con esa descripción básica. Sin embargo, nosotros estamos interesados solamente en tres de esos tipos e ignoraremos por ahora el grupo llamado 'intermedio', que contiene aquellas fibras cuyas características no corresponden claramente a ninguno de los otros tres grupos. Estos tipos de fibras son las lentas (tipo I) y las rápidas (tipos IIA y IIB). 3. Fibras lentas (tipo I) Este es el tipo mas característico de fibra, ya que todas tienen diámetros pequeños, sacudidas de larga duración, fuerza máxima de poca amplitud y una gran resistencia a la fatiga (Tabla I). Desde el punto de vista bioquímico, tienen un gran contenido de enzimas oxidativas, con pocos marcadores glicolíticos y baja actividad ATPásica. Contienen grandes cantidades de mioglobina que puede ayudarles a amortiguar los niveles de oxígeno durante periodos de ejercicio extremo y su pequeño diámetro puede ser una adaptación para permitir la difusión rápida del oxígeno y bióxido de carbono. Estas fibras se han llamado lentas u oxidativas lentas. 4. Fibras rápidas (tipo II) Sobre la base de su resistencia a la fatiga, las fibras musculares rápidas pueden dividirse en dos grupos, A y B. Las fibras del grupo A también son llamadas de tipo IIa y son poco frecuentes en el humano. Tienen sacudidas rápidas de corta duración, son relativamente resistentes a la fatiga (Tabla I) y tienden a tener altas concentraciones de enzimas oxidativas y glicolíticas, así como una actividad ATPásica alta. Se han llamado Resistentes Rápidas (Fast Resistant, FR) u Oxidativas-Glicolíticas Rápidas (Fast Oxidative-Glycolytic, FOG). Generalmente las fibras del grupo B son llamadas tipo IIb y tienen sacudidas muy rápidas de corta duración, que en comparación con las fibras de tipo I generan una gran
- 19. fuerza, aunque no pueden mantenerla durante mas de unas pocas contracciones. Si son estimuladas por periodos largos de tiempo su tensión activa disminuye y el músculo muestra fatiga (Tabla I). Tienen tazas ATPásicas altas (por ello las velocidades rápidas de la sacudida), actividades glicolíticas altas y capacidad oxidativa baja. También tienen poca hemolobina (por lo que se ven de color claro), una densidad baja de mitocondrias y tienden a una densidad baja de capilares. Estas fibras también se han llamado Fatigables Rápidas (Fast Fatigable, FF) o Glicolíticas Rápidas (Fast Glycolytic, FG). Tabla I. Comparación de las principales propiedades de los dos tipos de unidades motoras histoquímicamente diferentes 5. ¿Qué determina el tipo de fibra muscular? Al nacimiento la mayor parte de los músculos están compuestos por músculos lentos (de tipo I) y es durante la maduración que se llega a la proporción final de músculos rápidos y lentos. Por ello, es probable que el tipo de fibra muscular sea determinado por la inervación y aunque puede haber efectos tróficos del nervio mismo (quizá un compuesto antigénico), parece que el patrón de actividad tiene una gran influencia en la determinación de muchas de las propiedades características del músculo.
- 20. Si un músculo lento (cuyo nervio motor generalmente dispara a baja frecuencias durante largos periodos de tiempo) es estimulado en el laboratorio con descargas de alta frecuencia (semejante a las que se observan en las fibras rápidas), empieza a mostrar muchas de las propiedades de las fibras rápidas. Mas aún, si se denerva un músculo lento y después se reinerva con un axón motor rápido (como el que inerva las fibras rápidas), sus fibras llegan a mostrar todas las características de las fibras rápidas.