Quimica
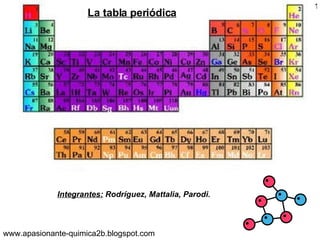
- 1. www.apasionante-quimica2b.blogspot.com 1 Integrantes: Rodríguez, Mattalia, Parodi. La tabla periódica
- 2. CONSIGNAS 2 http://apasionante-química2b Pág. 3 y 4
- 3. b) 3 http://apasionante-química2b I. Es un gas no reactivo a temperatura ambiente; se lo utiliza en carteles de publicidad y lámparas. VII. Es un gas que no reacciona, se lo utiliza en lámparas y tiene 18 protones y 8 electrones en su último nivel energético. II. Es un sólido negro; puede presentarse en diversas formas pero las más comunes son el grafito y el diamante. Su estructura es gigante, es decir que forma una red tridimensional con sus átomos. IX. Es uno de los elementos presentes en la arena y las siliconas. Tiene una estructura gigante. III. Es el gas necesario para que ocurra la combustión de cualquier sustancia. Constituye el 21% del aire y tiene 6 electrones en su último nivel. VIII. Es un sólido amarillo que se vende en las farmacias en forma de barritas. Se lo extrae de depósitos bajo la tierra y volcanes. Tiene 6 electrones en la última capa.
- 4. b) 4 http://apasionante-química2b IV. Es un sólido cuyos átomos tienen 5 electrones en su última capa. Forma un compuesto que se llama fosfina. VI. Es el gas más abundante en el aire, no conduce electricidad y tiene 5 electrones en su última capa. Es uno de los elementos presentes en el amoníaco V. Es un gas que reacciona rápidamente con el sodio para formar un compuesto que se encuentra en la pasta de dientes X. Es muy reactivo; por eso, se encuentra formando compuestos con otros elementos en la naturaleza. Uno de estos compuestos, la sal de mesa, lo forma con el sodio
- 5. c) 5 http://apasionante-química2b I. Neón II. Carbono III. Oxigeno IV. Fósforo V. Fluor VI. Nitrógeno VII. Argón VIII. Azufre IX. Silicio X. Cloro Grupo 18 Grupo 14 Grupo 16 Grupo 15 Grupo 17 Grupo 15 Grupo 18 Grupo 16 Grupo 14 Grupo 17
- 6. d) 1. La relación que existe entre el nº de electrones del último nivel energético de un elemento y el nº de grupo que ocupa en la tabla es que los elementos de un mismo grupo tienen la misma cantidad de e- en su ultimo nivel y por lo tanto propiedades similares. 2. El nº de protones y la posición del elemento en la tabla se relacionan en que el NºZ (nº de protones) es el que determina la posición en la tabla en forma creciente; y el nº de electrones es igual al de protones ya que por cada p+ tiene que haber un e-. 3. La particularidad en la configuración electrónica de los gases nobles es que tienen todos los niveles completos a excepción del helio; a causa de eso es más difícil agregar o sustraer electrones, es decir, que no se mezclan con otros elementos. 6 http://apasionante-química2b