7 saberes para la educación del futuro por edgar morín
•Descargar como DOCX, PDF•
0 recomendaciones•313 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Los 7 saberes de la educación

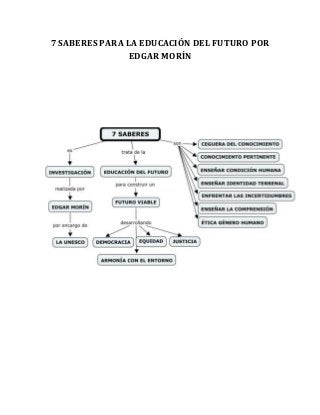
El documento presenta 7 saberes o formas de enseñanza necesarias para la educación del futuro: 1) reconocer errores y ilusiones, 2) principios de conocimiento relevante, 3) enseñar la condición humana, 4) identidad terrenal, 5) enfrentar incertidumbres, 6) enseñar comprensión, y 7) ética del género humano. Los autores buscan generar docentes capacitados y transformar la educación para preparar a los estudiantes para un mundo en constante cambio.
Los 7 saberes necesarios para la educación del futuro

Con base en el texto los 7 saberes necesarios para la educación de Edgar Morin se realizó esta presentación que expone los puntos más relevantes de la lectura.
Proyecto quimica

Este proyecto busca demostrar reacciones químicas sencillas como la neutralización entre el vinagre (ácido acético) y el bicarbonato sódico usando bolitas de naftalina que suben y bajan en el líquido debido a las burbujas de dióxido de carbono generadas. El objetivo es que los estudiantes puedan verificar conceptos químicos de manera práctica y sencilla sin necesidad de un laboratorio completo.
Taller. qimc2

1) El documento presenta 17 preguntas relacionadas con conceptos químicos como números atómicos, isótopos, iones, estructura atómica, tabla periódica y enlaces químicos. 2) Algunas preguntas piden identificar propiedades de elementos como su grupo y período, calcular números de masa de isótopos, y determinar el tipo de enlace en diferentes moléculas. 3) Las preguntas abarcan una variedad de temas químicos fundamentales.
Exposicion sales oxisales

Este documento describe los diferentes tipos de sales, incluyendo sales ácidas, básicas, dobles, neutras y mixtas. Explica cómo se forman y cómo se nombran, con ejemplos como el sulfato de sodio, el sulfato de férrico y el sulfato de plata.
áTomo

El documento describe la evolución de los modelos atómicos, incluyendo el modelo de Dalton, Thomson, Rutherford y Bohr. Dalton propuso que la materia está compuesta de átomos indivisibles que se combinan en proporciones simples. Rutherford descubrió el núcleo atómico. Bohr propuso que los electrones orbitan el núcleo en órbitas cuantizadas.
Materia

La química es la ciencia que estudia la materia y sus transformaciones. Se divide en química general, inorgánica, orgánica y aplicada. Estudia las propiedades y cambios de la materia, incluyendo su clasificación en elementos, compuestos y mezclas. También examina conceptos como masa, peso, volumen y las unidades de medida asociadas a estos.
Equilibrio ionico

Este documento describe los conceptos fundamentales de los electrolitos y el equilibrio iónico en soluciones acuosas. Explica que los electrolitos fuertes se disocian completamente en iones, mientras que los débiles lo hacen parcialmente. También define el pH y pOH y describe cómo medir la concentración de iones hidrógeno y hidroxilo. Por último, analiza los efectos de la hidrólisis en medios ácidos, básicos o neutros.
Recomendados
Los 7 saberes de la educación

El documento presenta 7 saberes o formas de enseñanza necesarias para la educación del futuro: 1) reconocer errores y ilusiones, 2) principios de conocimiento relevante, 3) enseñar la condición humana, 4) identidad terrenal, 5) enfrentar incertidumbres, 6) enseñar comprensión, y 7) ética del género humano. Los autores buscan generar docentes capacitados y transformar la educación para preparar a los estudiantes para un mundo en constante cambio.
Los 7 saberes necesarios para la educación del futuro

Con base en el texto los 7 saberes necesarios para la educación de Edgar Morin se realizó esta presentación que expone los puntos más relevantes de la lectura.
Proyecto quimica

Este proyecto busca demostrar reacciones químicas sencillas como la neutralización entre el vinagre (ácido acético) y el bicarbonato sódico usando bolitas de naftalina que suben y bajan en el líquido debido a las burbujas de dióxido de carbono generadas. El objetivo es que los estudiantes puedan verificar conceptos químicos de manera práctica y sencilla sin necesidad de un laboratorio completo.
Taller. qimc2

1) El documento presenta 17 preguntas relacionadas con conceptos químicos como números atómicos, isótopos, iones, estructura atómica, tabla periódica y enlaces químicos. 2) Algunas preguntas piden identificar propiedades de elementos como su grupo y período, calcular números de masa de isótopos, y determinar el tipo de enlace en diferentes moléculas. 3) Las preguntas abarcan una variedad de temas químicos fundamentales.
Exposicion sales oxisales

Este documento describe los diferentes tipos de sales, incluyendo sales ácidas, básicas, dobles, neutras y mixtas. Explica cómo se forman y cómo se nombran, con ejemplos como el sulfato de sodio, el sulfato de férrico y el sulfato de plata.
áTomo

El documento describe la evolución de los modelos atómicos, incluyendo el modelo de Dalton, Thomson, Rutherford y Bohr. Dalton propuso que la materia está compuesta de átomos indivisibles que se combinan en proporciones simples. Rutherford descubrió el núcleo atómico. Bohr propuso que los electrones orbitan el núcleo en órbitas cuantizadas.
Materia

La química es la ciencia que estudia la materia y sus transformaciones. Se divide en química general, inorgánica, orgánica y aplicada. Estudia las propiedades y cambios de la materia, incluyendo su clasificación en elementos, compuestos y mezclas. También examina conceptos como masa, peso, volumen y las unidades de medida asociadas a estos.
Equilibrio ionico

Este documento describe los conceptos fundamentales de los electrolitos y el equilibrio iónico en soluciones acuosas. Explica que los electrolitos fuertes se disocian completamente en iones, mientras que los débiles lo hacen parcialmente. También define el pH y pOH y describe cómo medir la concentración de iones hidrógeno y hidroxilo. Por último, analiza los efectos de la hidrólisis en medios ácidos, básicos o neutros.
Equilibrio quìmico

El documento describe los conceptos de cinética química y equilibrio químico. Explica cómo la velocidad de formación de un producto iguala la velocidad de descomposición cuando se alcanza el equilibrio químico. También define la constante de equilibrio Kc en términos de concentraciones molares y la constante de equilibrio Kp en términos de presiones parciales. Muestra ejemplos de cómo calcular Kc y Kp para diferentes reacciones químicas.
Sistemas dispersos

La solución es una mezcla homogénea de dos o más componentes que no tienden a separarse y cuyas propiedades son una combinación de las propiedades de sus componentes. Las soluciones se pueden expresar mediante porcentajes en masa o volumen, concentración molar, normalidad o molalidad. Las soluciones exhiben propiedades coligativas como el aumento de la temperatura de ebullición, disminución de la temperatura de congelación y disminución de la presión de vapor.
Balanceo de ecuaciones químicas

Este documento presenta varios métodos para balancear ecuaciones químicas, incluyendo el método de tanteo, el intercambio de números de oxidación, y el método de semiecuaciones. Explica las reglas para determinar números de oxidación y cómo usar los números de oxidación para balancear ecuaciones redox mediante el intercambio de electrones ganados y perdidos. También proporciona ejemplos detallados del uso de estos métodos para balancear varias ecuaciones químicas.
Ecuaciones químicas de oxi-red

Este documento trata sobre las ecuaciones químicas de óxido-reducción. Explica que la oxidación es la pérdida de electrones, mientras que la reducción es la ganancia de electrones. Como ejemplo, presenta la reacción de oxidación del hierro donde el Fe pasa de un estado de oxidación 0 a +3 al combinarse con el oxígeno. También describe las reglas para determinar los números de oxidación de los átomos en una molécula.
Ecuaciones químicas

Este documento resume los conceptos básicos de las ecuaciones químicas, incluyendo las sustancias simples y compuestas, las reacciones químicas y ecuaciones, y las clasificaciones de reacciones como formación, descomposición, sustitución y doble sustitución. También describe las reacciones endotérmicas y exotérmicas, y la ley de conservación de la materia.
Relaciones cuantitativas

Este documento discute conceitos químicos fundamentais como mol, número de Avogadro, peso atômico, peso molecular e suas aplicações em cálculos químicos. Explica como calcular a fórmula empírica e molecular de compostos a partir de sua composição percentual e pesos atômicos dos elementos. Fornece exemplos de cálculos para compostos como NaNO3, H3PO4 e C4H10.
Nomenclatura

Este documento trata sobre la nomenclatura de compuestos inorgánicos. Explica los sistemas para nombrar compuestos binarios como cloruro de sodio, compuestos ternarios como sales formadas por la reacción de ácidos y bases, y diferentes tipos de compuestos como hidruros, óxidos, ácidos y sales. También describe conceptos fundamentales como valencia electrónica, tabla periódica y tipos de radicales presentes en compuestos.
Tabla periodica

Este documento presenta la tabla periódica y describe sus características principales como los metales y no metales, los bloques, los grupos y los períodos. Explica que los elementos se ordenan de acuerdo con sus números atómicos y que las propiedades van cambiando periódicamente a lo largo de los períodos pero son similares dentro de los grupos.
Radiación electromagnética

La radiación electromagnética incluye diferentes tipos como microondas, rayos X, ondas de radio, rayos ultravioleta e infrarrojos, y luz visible. Es una forma de energía que se desplaza en forma de ondas sin necesidad de conductores. El espectroscopio separa la luz blanca en un espectro de colores utilizando una rendija y un prisma, lo que permite estudiar las longitudes de onda de la radiación electromagnética. La energía de un fotón depende de su longitud de onda y la constante de
Configuración electrónica

El documento describe la configuración electrónica según los postulados de Bohr. Bohr propuso que los electrones giran en órbitas definidas alrededor del núcleo, y que para pasar de una órbita a otra deben absorber o emitir energía. Las órbitas más alejadas del núcleo tienen mayor energía.
Teorias atomicas

Este documento presenta las principales teorías atómicas a través de la historia, incluyendo las teorías de Dalton, Thomson, Rutherford y Bohr. Explica los modelos atómicos propuestos por cada científico, como la idea de Dalton de que los átomos son las unidades fundamentales de la materia, el modelo de Thomson del átomo como una esfera de carga positiva con electrones incrustados, y el modelo planetario de Rutherford que propuso la existencia de un núcleo central.
Modelo atòmico de Bohr

El modelo atómico de Bohr propuso que: 1) los electrones orbitan en órbitas definidas alrededor del núcleo a radios fijos; 2) la energía de las órbitas es estacionaria; y 3) para que un electrón cambie de órbita, debe absorber o emitir energía en un cuántico igual a la diferencia de energía entre las dos órbitas.
Taller 4

El documento contiene varios problemas de física relacionados con conceptos como velocidad media, aceleración, desplazamiento y rapidez. Incluye preguntas sobre un automóvil que da una vuelta a una pista circular, sobre cuáles de varios enunciados son falsos, y sobre el movimiento y aceleración de diferentes objetos en gráficos y diagramas de posición vs tiempo.
Taller 3

Este documento presenta 20 problemas de conversión de unidades y cálculos con unidades, incluyendo conversiones entre kilómetros y metros, microgramos a kilogramos, kilómetros por minuto a metros por segundo, y operaciones como sumas y divisiones con unidades. El documento proporciona un taller práctico de nivelación sobre conceptos físicos básicos de unidades y conversión.
Taller 05

El documento contiene varios problemas y preguntas relacionadas con conceptos de física como velocidad, aceleración y movimiento. Incluye preguntas sobre la velocidad promedio de un auto en una pista circular, cuáles de varios enunciados sobre velocidad y aceleración son falsos, y la velocidad promedio de un corredor más rápido al alcanzar a otro corredor.
Cinematica

1) La cinemática estudia los movimientos de los cuerpos independientemente de las causas que los producen. 2) La velocidad es una magnitud física vectorial que expresa la distancia recorrida por un objeto por unidad de tiempo. 3) La velocidad media se calcula dividiendo el desplazamiento total entre el tiempo empleado, mientras que la velocidad instantánea representa la velocidad en un punto de la trayectoria.
Cinemática en una dimensión

El documento describe cómo la física se subdividió en diversas ramas para estudiar fenómenos relacionados, incluyendo la mecánica, termodinámica, óptica, electromagnetismo y física moderna. Luego explica conceptos clave de la cinemática como posición, desplazamiento, velocidad, aceleración y su representación y cálculo.
Taller 2 cifras significativas 

Este documento presenta una serie de ejercicios sobre cifras significativas y notación científica. Se pide identificar la forma correcta de escribir varios valores numéricos dados en notación científica, incluyendo medidas como la masa del sol, la altura del Monte Everest, y el periodo de vibración de una cuerda de guitarra. El objetivo es practicar la expresión de valores usando la notación científica de manera apropiada considerando el número de cifras significativas.
Taller 1 conversiones de unidades

Este documento presenta 20 problemas de física sobre conversiones de unidades de longitud, masa, tiempo e velocidad. Los problemas incluyen conversiones entre kilómetros, metros, hectómetros, decímetros, centímetros, milímetros, gramos, kilogramos, horas, minutos, segundos y años.
Leyes de newton

Este documento explica los conceptos fundamentales de la dinámica, incluyendo las leyes del movimiento de Newton. Describe las diferencias entre cinemática y dinámica, y cómo Newton resumió los principios del movimiento en tres leyes. También define conceptos clave como fuerza, masa, peso e inercia, y cómo estas cantidades se relacionan según las leyes de Newton.
Más contenido relacionado
Más de Cristina Cotera
Equilibrio quìmico

El documento describe los conceptos de cinética química y equilibrio químico. Explica cómo la velocidad de formación de un producto iguala la velocidad de descomposición cuando se alcanza el equilibrio químico. También define la constante de equilibrio Kc en términos de concentraciones molares y la constante de equilibrio Kp en términos de presiones parciales. Muestra ejemplos de cómo calcular Kc y Kp para diferentes reacciones químicas.
Sistemas dispersos

La solución es una mezcla homogénea de dos o más componentes que no tienden a separarse y cuyas propiedades son una combinación de las propiedades de sus componentes. Las soluciones se pueden expresar mediante porcentajes en masa o volumen, concentración molar, normalidad o molalidad. Las soluciones exhiben propiedades coligativas como el aumento de la temperatura de ebullición, disminución de la temperatura de congelación y disminución de la presión de vapor.
Balanceo de ecuaciones químicas

Este documento presenta varios métodos para balancear ecuaciones químicas, incluyendo el método de tanteo, el intercambio de números de oxidación, y el método de semiecuaciones. Explica las reglas para determinar números de oxidación y cómo usar los números de oxidación para balancear ecuaciones redox mediante el intercambio de electrones ganados y perdidos. También proporciona ejemplos detallados del uso de estos métodos para balancear varias ecuaciones químicas.
Ecuaciones químicas de oxi-red

Este documento trata sobre las ecuaciones químicas de óxido-reducción. Explica que la oxidación es la pérdida de electrones, mientras que la reducción es la ganancia de electrones. Como ejemplo, presenta la reacción de oxidación del hierro donde el Fe pasa de un estado de oxidación 0 a +3 al combinarse con el oxígeno. También describe las reglas para determinar los números de oxidación de los átomos en una molécula.
Ecuaciones químicas

Este documento resume los conceptos básicos de las ecuaciones químicas, incluyendo las sustancias simples y compuestas, las reacciones químicas y ecuaciones, y las clasificaciones de reacciones como formación, descomposición, sustitución y doble sustitución. También describe las reacciones endotérmicas y exotérmicas, y la ley de conservación de la materia.
Relaciones cuantitativas

Este documento discute conceitos químicos fundamentais como mol, número de Avogadro, peso atômico, peso molecular e suas aplicações em cálculos químicos. Explica como calcular a fórmula empírica e molecular de compostos a partir de sua composição percentual e pesos atômicos dos elementos. Fornece exemplos de cálculos para compostos como NaNO3, H3PO4 e C4H10.
Nomenclatura

Este documento trata sobre la nomenclatura de compuestos inorgánicos. Explica los sistemas para nombrar compuestos binarios como cloruro de sodio, compuestos ternarios como sales formadas por la reacción de ácidos y bases, y diferentes tipos de compuestos como hidruros, óxidos, ácidos y sales. También describe conceptos fundamentales como valencia electrónica, tabla periódica y tipos de radicales presentes en compuestos.
Tabla periodica

Este documento presenta la tabla periódica y describe sus características principales como los metales y no metales, los bloques, los grupos y los períodos. Explica que los elementos se ordenan de acuerdo con sus números atómicos y que las propiedades van cambiando periódicamente a lo largo de los períodos pero son similares dentro de los grupos.
Radiación electromagnética

La radiación electromagnética incluye diferentes tipos como microondas, rayos X, ondas de radio, rayos ultravioleta e infrarrojos, y luz visible. Es una forma de energía que se desplaza en forma de ondas sin necesidad de conductores. El espectroscopio separa la luz blanca en un espectro de colores utilizando una rendija y un prisma, lo que permite estudiar las longitudes de onda de la radiación electromagnética. La energía de un fotón depende de su longitud de onda y la constante de
Configuración electrónica

El documento describe la configuración electrónica según los postulados de Bohr. Bohr propuso que los electrones giran en órbitas definidas alrededor del núcleo, y que para pasar de una órbita a otra deben absorber o emitir energía. Las órbitas más alejadas del núcleo tienen mayor energía.
Teorias atomicas

Este documento presenta las principales teorías atómicas a través de la historia, incluyendo las teorías de Dalton, Thomson, Rutherford y Bohr. Explica los modelos atómicos propuestos por cada científico, como la idea de Dalton de que los átomos son las unidades fundamentales de la materia, el modelo de Thomson del átomo como una esfera de carga positiva con electrones incrustados, y el modelo planetario de Rutherford que propuso la existencia de un núcleo central.
Modelo atòmico de Bohr

El modelo atómico de Bohr propuso que: 1) los electrones orbitan en órbitas definidas alrededor del núcleo a radios fijos; 2) la energía de las órbitas es estacionaria; y 3) para que un electrón cambie de órbita, debe absorber o emitir energía en un cuántico igual a la diferencia de energía entre las dos órbitas.
Taller 4

El documento contiene varios problemas de física relacionados con conceptos como velocidad media, aceleración, desplazamiento y rapidez. Incluye preguntas sobre un automóvil que da una vuelta a una pista circular, sobre cuáles de varios enunciados son falsos, y sobre el movimiento y aceleración de diferentes objetos en gráficos y diagramas de posición vs tiempo.
Taller 3

Este documento presenta 20 problemas de conversión de unidades y cálculos con unidades, incluyendo conversiones entre kilómetros y metros, microgramos a kilogramos, kilómetros por minuto a metros por segundo, y operaciones como sumas y divisiones con unidades. El documento proporciona un taller práctico de nivelación sobre conceptos físicos básicos de unidades y conversión.
Taller 05

El documento contiene varios problemas y preguntas relacionadas con conceptos de física como velocidad, aceleración y movimiento. Incluye preguntas sobre la velocidad promedio de un auto en una pista circular, cuáles de varios enunciados sobre velocidad y aceleración son falsos, y la velocidad promedio de un corredor más rápido al alcanzar a otro corredor.
Cinematica

1) La cinemática estudia los movimientos de los cuerpos independientemente de las causas que los producen. 2) La velocidad es una magnitud física vectorial que expresa la distancia recorrida por un objeto por unidad de tiempo. 3) La velocidad media se calcula dividiendo el desplazamiento total entre el tiempo empleado, mientras que la velocidad instantánea representa la velocidad en un punto de la trayectoria.
Cinemática en una dimensión

El documento describe cómo la física se subdividió en diversas ramas para estudiar fenómenos relacionados, incluyendo la mecánica, termodinámica, óptica, electromagnetismo y física moderna. Luego explica conceptos clave de la cinemática como posición, desplazamiento, velocidad, aceleración y su representación y cálculo.
Taller 2 cifras significativas 

Este documento presenta una serie de ejercicios sobre cifras significativas y notación científica. Se pide identificar la forma correcta de escribir varios valores numéricos dados en notación científica, incluyendo medidas como la masa del sol, la altura del Monte Everest, y el periodo de vibración de una cuerda de guitarra. El objetivo es practicar la expresión de valores usando la notación científica de manera apropiada considerando el número de cifras significativas.
Taller 1 conversiones de unidades

Este documento presenta 20 problemas de física sobre conversiones de unidades de longitud, masa, tiempo e velocidad. Los problemas incluyen conversiones entre kilómetros, metros, hectómetros, decímetros, centímetros, milímetros, gramos, kilogramos, horas, minutos, segundos y años.
Leyes de newton

Este documento explica los conceptos fundamentales de la dinámica, incluyendo las leyes del movimiento de Newton. Describe las diferencias entre cinemática y dinámica, y cómo Newton resumió los principios del movimiento en tres leyes. También define conceptos clave como fuerza, masa, peso e inercia, y cómo estas cantidades se relacionan según las leyes de Newton.
Más de Cristina Cotera (20)
7 saberes para la educación del futuro por edgar morín
- 1. 7 SABERES PARA LA EDUCACIÓN DEL FUTURO POR EDGAR MORÍN
