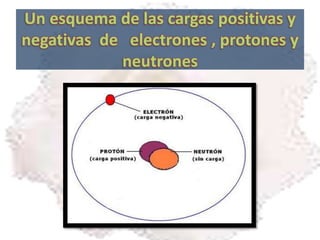
Un átomo es la menor cantidad de un elemento químico que tiene existencia propia y no puede dividirse mediante procesos químicos. Está formado por un núcleo central con protones y neutrones, alrededor del cual giran los electrones en órbitas de energía creciente. La molécula es la unión de dos o más átomos que comparten electrones y puede existir en estado sólido, líquido o gaseoso.