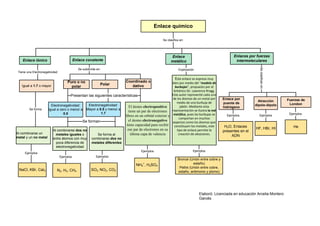
Este documento clasifica los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes, metálicos e intermoleculares. Describe las características de cada tipo de enlace, como la electronegatividad de los átomos involucrados y los ejemplos comunes de cada uno. También explica el modelo de "burbujas" para representar el enlace metálico.