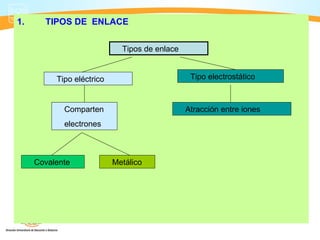
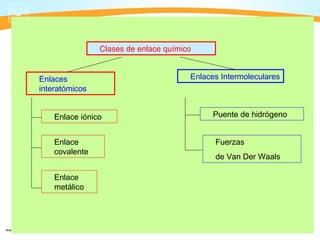
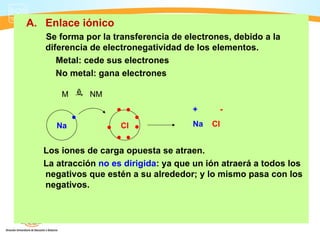
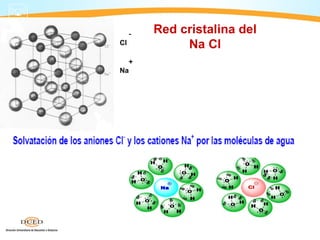
Este documento presenta información sobre los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes y metálicos. También discute las fuerzas intermoleculares como puentes de hidrógeno y fuerzas de Van der Waals. Finalmente, explica conceptos clave como electronegatividad y la teoría de Lewis sobre la formación de enlaces químicos.