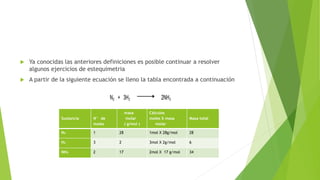
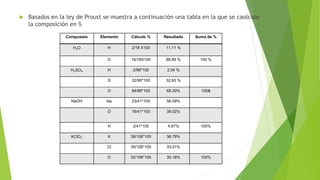
Este documento introduce los conceptos fundamentales de la estequiometría, incluyendo la definición, los pasos para resolver problemas, y las definiciones clave de masa atómica, masa molecular, masa molar, mol y la ley de Proust. Además, presenta ejemplos numéricos para ilustrar los cálculos estequiométricos.