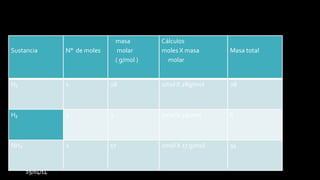
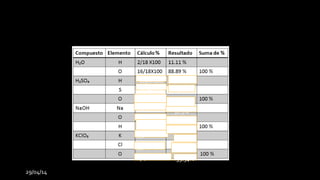
Este documento trata sobre la estequiometría. Explica que la estequiometría se utiliza para determinar las cantidades de reactivos y productos que intervienen en una reacción química. Luego, describe los pasos fundamentales para resolver problemas estequiométricos, que incluyen escribir la ecuación química, balancearla y calcular las masas, moles o moléculas de las sustancias mencionadas. Finalmente, presenta un ejemplo numérico para ilustrar cómo calcular las masas de cada sustancia.